インビラーゼカプセル200mg/インビラーゼ錠500mgの添付文書
ホーム > おくすりガイド > インビラーゼカプセル200mg/インビラーゼ錠500mg

| 商品名: | インビラーゼカプセル200mg インビラーゼ錠500mg |
|---|---|
| 一般名: | サキナビル |
| 略称 : | SQV |
添付文書の読み方
ここで提供している添付文書情報は、2011年4月18日現在の各医薬品の添付文書を基に作成したものです。書式等については、実際の添付文書と異なるところがあります。添付文書情報は随時更新されます。ご使用の際は、必ず最新の添付文書をご覧下さい。
また、記載されている内容には、専門的な情報が含まれています。文書内の、
この色の文字をクリックすると、別ウィンドウに読み方のアドバイスが表示されます。
この色の文字をクリックすると、別ウィンドウに重大な副作用の解説が表示されます。
この色の文字をクリックすると、別ウィンドウに副作用の症状とその類似語、定義の解説が表示されます。
記載されている情報をご覧になり、疑問などを持たれた場合は、医師・薬剤師にご相談ください。
※このページを開いた時に目次が自動的に表示されなかったときは、ここをクリックしてください。
HIVプロテアーゼ阻害剤

サキナビルメシル酸塩製剤
2011年3月改訂(第4版)
日本標準商品分類番号
87625
- 規制区分
- 劇薬
- 処方せん医薬品注1)
- 貯法
- カプセル―遮光、室温保存
- 錠―室温保存
- 使用期限
- カプセル―3年
- 錠―3年
- (外箱に表示の使用期限内に使用すること)
注1)注意-医師等の処方せんにより使用すること
| カプセル200mg | 錠500mg | |
|---|---|---|
| 承認番号 | 21700AMX00131 | 21800AMX10847 |
| 薬価収載 | 2006年6月 | 2006年9月 |
| 販売開始 | 1997年9月 | 2006年9月 |
| 国際誕生 | 1995年12月 | |
【禁忌(次の患者には投与しないこと)】
- 本剤又はリトナビル製剤の成分に対し過敏症の既往歴のある患者
- 重度の肝機能障害のある患者[B型・C型肝炎又は肝硬変等の肝疾患のある患者で、本剤投与中に門脈圧の上昇や肝疾患が悪化し、中には重篤な転帰をたどったとの報告がある。]
- QT延長のある患者(先天性QT延長症候群等)[QT延長や心室性不整脈を起こすおそれがある。]
- 低カリウム血症又は低マグネシウム血症のある患者[QT延長や心室性不整脈を起こすおそれがある。]
- ペースメーカーを装着していない完全房室ブロックの患者
- 次の薬剤を投与中の患者:アミオダロン、フレカイニド、プロパフェノン、ベプリジル、キニジン、トラゾドン、ピモジド、エルゴタミン製剤、シンバスタチン、ミダゾラム、トリアゾラム、リファンピシン、バルデナフィル、アゼルニジピン含有製剤(「相互作用」の項参照)
【組成・性状】
| インビラーゼカプセル200mg | 成分 (1カプセル中) |
有効成分・含有量 | サキナビルメシル酸塩 228.7 mg (サキナビルとして200mg) |
||||
|---|---|---|---|---|---|---|---|
| 添加物 | 内容物:無水乳糖、結晶セルロース、ポビドン、デンプングリコール酸ナトリウム、タルク、ステアリン酸マグネシウム カプセル:ゼラチン、黒酸化鉄、黄色三二酸化鉄、三二酸化鉄、酸化チタン、食用青色2号、ラウリル硫酸ナトリウム |
||||||
| 色 | キャップ | 緑色 | |||||
| ボディー | 淡褐色 | ||||||
| 剤形 | 硬カプセル(0号) | ||||||
| 外形 | |||||||
| 平均重量 | 約505mg | ||||||
| インビラーゼ錠500mg | 成分(1錠中) | 有効成分・含有量 | サキナビルメシル酸塩 571.5mg(サキナビルとして500mg) | ||||
| 添加物 | 乳糖水和物、ポビドン、クロスカルメロースナトリウム、結晶セルロース、ステアリン酸マグネシウム、ヒプロメロース、タルク、酸化チタン、黄色三二酸化鉄、三二酸化鉄、トリアセチン | ||||||
| 色 | うすい黄赤色~明るい灰黄赤色又はうすい赤みの黄色 | ||||||
| 剤形 | フィルムコート錠 | ||||||
| 外形 | 平面 | 側面 | |||||
 |
 |
||||||
| 長径 | 約19.0mm | ||||||
| 短径 | 約8.9mm | ||||||
| 厚さ | 約7.2mm | ||||||
| 平均重量 | 約820mg | ||||||
【効能・効果】
HIV感染症
【用法・用量】
通常、成人には、サキナビルとして1回1,000mgを1日2回、リトナビルとして1回100mgを1日2回、同時に、食後2時間以内に経口投与する。
投与に際しては必ず他の抗HIV薬と併用すること。
〈用法・用量に関連する使用上の注意〉
リトナビル及び他の抗HIV薬との併用に際しては、併用薬剤の用法・用量、使用上の注意等を必ず確認すること。
【使用上の注意】
1.慎重投与(次の患者には慎重に投与すること)
- 血友病患者及び著しい出血傾向を有する患者[本剤投与により、突発性の皮下血腫や出血性関節症等の出血事象の増加が血友病患者で報告されている。]
- 中等度の肝機能障害のある患者[本剤の血中濃度が上昇するおそれがある。]
- 重度の腎機能障害のある患者(【薬物動態】の項参照)
- 重度の徐脈等の不整脈、心疾患(虚血性心疾患、心筋症等)のある患者[QT延長や心室性不整脈を起こすおそれがある。]
- 高齢者(「高齢者への投与」の項参照)
2.重要な基本的注意
- 本剤の使用に際しては、患者又はそれに代わる適切な者に、次の事項についてよく説明し同意を得た後、使用すること。
- 本剤はHIV感染症の根治療法薬ではないことから、日和見感染を含むHIV感染症の進展に伴う疾病を発症し続ける可能性があるので、本剤投与開始後の身体状況の変化については、すべて担当医師に報告すること。
- 本剤の長期投与による影響については、現在のところ不明であること。
- 本剤による治療が、性的接触又は血液汚染等による他者へのHIV感染の危険を減少させることは明らかではないこと。
- 本剤を空腹時に服用すると血中濃度が低くなり抗ウイルス作用を発揮できないことがあるため、本剤とリトナビルは食後2時間以内に同時に服用すること。
- 用量依存性のQT延長、PR延長が起こるおそれがあるため、不整脈が疑われる徴候や症状(動悸、失神等)があらわれた場合には、速やかに担当医師に報告すること。
- 担当医師の指示なしに用量を変更したり、服用を中止したりしないこと。
- 本剤は併用薬剤と相互作用を起こすことがあるため、服用中のすべての薬剤を担当医師に報告すること(「相互作用」の項参照)。また、本剤で治療中に新たに他の薬剤を服用する場合には、事前に担当医師に相談すること。
- 本剤投与によりQT延長が起こるおそれがあることから、本剤の投与を開始する前に心血管系の状態に注意し、本剤投与中に不整脈の徴候があらわれた場合には心電図検査を行い、QT延長、PR延長が認められた場合には本剤の投与を中止するなど適切な処置を行うこと。
- 本剤を含むHIVプロテアーゼ阻害剤の投与により、糖尿病の発症又は悪化が起こり、ケトアシドーシスに至った症例も報告されているため、定期的な検査等を行うこと。
- 抗HIV薬の使用により、体脂肪の再分布/蓄積があらわれることがあるので、異常が認められた場合には適切な処置を行うこと(「その他の副作用」の項参照)。
- 本剤を含む抗HIV薬の多剤併用療法を行った患者で、免疫再構築症候群が報告されている。投与開始後、免疫機能が回復し、症候性のみならず無症候性日和見感染(マイコバクテリウムアビウムコンプレックス、サイトメガロウイルス、ニューモシスチス等によるもの)等に対する炎症反応が発現することがあるので、これらの炎症性の症状を評価し、必要時には適切な治療を考慮すること。
- リトナビルの用量の増加に伴い副作用が増加したとの報告がある。ときに、リトナビルとの併用により、重度の副作用、主に糖尿病性ケトアシドーシス、肝機能障害(特に肝疾患の既往歴のある患者)が報告されているので観察を十分に行うこと。
3.相互作用
本剤は、肝薬物代謝酵素チトクロームP450(CYP3A4)によって代謝される。更に本剤はP-糖蛋白の基質である。これらと親和性のある薬剤の血中濃度に影響を与えることがある(【薬物動態】の項参照)。
(1)併用禁忌(併用しないこと)
| 薬剤名等 | 臨床症状・措置方法 | 機序・危険因子 |
|---|---|---|
| アミオダロン (アンカロン) フレカイニド (タンボコール) プロパフェノン (プロノン) ベプリジル (ベプリコール) キニジン (硫酸キニジン) トラゾドン (デジレル、レスリン) ピモジド (オーラップ) |
左記の薬剤の血中濃度が増加し、重篤又は生命に危険を及ぼすような心血管系の副作用(QT延長等)を起こすおそれがある。 | チトクロームP450(CYP3A4)に対する競合による。 |
| エルゴタミン製剤 (カフェルゴット等) |
左記の薬剤の血中濃度が増加し、急性麦角中毒(末梢血管痙攣、四肢の虚血等)を起こすおそれがある。 | チトクロームP450(CYP3A4)に対する競合による。 |
| シンバスタチン (リポバス) |
左記の薬剤の血中濃度が増加し、横紋筋融解症等のミオパシーを起こすおそれがある。 | チトクロームP450(CYP3A4)に対する競合による。 |
| ミダゾラム (ドルミカム) トリアゾラム (ハルシオン等) |
左記の薬剤の血中濃度が増加し、持続的又は過度の鎮静、呼吸抑制を起こすおそれがある。 ミダゾラムのクリアランスが減少し、半減期が延長したとの報告がある。 |
チトクロームP450(CYP3A4)に対する競合による。 |
| リファンピシン (アプテシン、リファジン、リマクタン等) |
本剤のAUCが減少したとの報告がある。 リファンピシンの投与を受けた患者に本剤を投与する場合には、少なくとも2週間の間隔をおくことが望ましい。 また、本剤/リトナビル/リファンピシンを併用した17例中11例(65%)が28日目までに重度の肝細胞毒性を発現したとの報告がある。 |
左記の薬剤はチトクロームP450(CYP3A4)を誘導する。 |
| バルデナフィル (レビトラ) |
左記の薬剤の血中濃度が増加するおそれがある。 | チトクロームP450(CYP3A4)に対する競合による。 |
| アゼルニジピン含有製剤 (カルブロック、レザルタス配合錠) |
左記の薬剤の血中濃度が増加するおそれがある。 | チトクロームP450(CYP3A4)に対する競合による。 |
(2)併用注意(併用に注意すること)
| 薬剤名等 | 臨床症状・措置方法 | 機序・危険因子 |
|---|---|---|
| デラビルジン | サキナビルメシル酸塩(600mg1日3回)とデラビルジン(400mg1日3回)を併用した場合に、サキナビルのAUCが348%、Cmaxが317%増加したとの報告がある。また、併用患者の13%で併用開始後数週間に肝細胞酵素が上昇したとの報告があるため、定期的に肝機能検査を行うことが望ましい。 | チトクロームP450(CYP3A4)に対する競合による。 |
| エファビレンツ | サキナビルとエファビレンツを併用した場合に、サキナビル及びエファビレンツのAUC、Cmaxが減少したとの報告がある。 サキナビル/リトナビル/エファビレンツ(1,600/200/600mg1日1回)を併用した場合に、サキナビル/リトナビル(1,600/200mg1日1回)併用した場合と比較して、サキナビルのAUC、Cmaxに影響がなかったとの報告がある。 サキナビル/リトナビル/エファビレンツ(1,200/100/600mg1日1回)を併用した場合又はサキナビルメシル酸塩/リトナビル(1,000/100mg1日2回)とエファビレンツ(600mg1日1回)を併用した場合に、サキナビル、エファビレンツの血中濃度に影響がなかったとの報告がある。 |
左記の薬剤は、チトクロームP450(CYP3A4)を誘導する。 |
| ネビラピン | サキナビルメシル酸塩(600mg1日3回)とネビラピン(200mg1日2回)を併用した場合に、サキナビルのAUCが24%減少したとの報告がある。 | 左記の薬剤は、チトクロームP450(CYP3A4)を誘導する。 |
| インジナビル | サキナビルメシル酸塩とインジナビルを併用した場合に、サキナビルのAUCが増加したとの報告がある。 | チトクロームP450(CYP3A4)に対する競合による。 |
| ネルフィナビル |
サキナビルとネルフィナビルを併用した場合に、サキナビル及びネルフィナビルのAUCが増加したとの報告がある。 併用により下痢が増加したとの報告がある。 |
チトクロームP450(CYP3A4)に対する競合による。 |
| アタザナビル | サキナビルメシル酸塩/リトナビル/アタザナビル(1,600/100/300mg1日1回)を併用した場合に、サキナビルメシル酸塩/リトナビル(1,600/100mg1日1回)を投与した場合と比較して、サキナビルのAUC、Cmaxがそれぞれ60%、42%、リトナビルのAUC、Cmaxがそれぞれ41%、34%増加したが、アタザナビルのAUC、Cmaxには影響をあたえなかったとの報告がある。 | 機序不明 |
| ホスアンプレナビル |
サキナビル(800mg1日3回)とアンプレナビル(750又は800mg1日3回)を併用した場合に、サキナビルのAUCが19%、アンプレナビルのAUCが32%減少したとの報告がある。 サキナビルメシル酸塩/リトナビル(1,000/100mg1日2回)とホスアンプレナビル(700mg1日2回)を併用した場合に、サキナビルのAUC、Cmaxがそれぞれ15%、9%減少したとの報告がある。 |
チトクロームP450(CYP3A4)に対する競合による。 |
| ロピナビル・リトナビル配合剤 |
サキナビル(1,200mg1日2回)とロピナビル/リトナビル(400/100mg1日2回)を併用した場合に、サキナビル単独投与の場合と比較して、サキナビルのAUC、Cmaxが増加したとの報告がある。 一方、サキナビル/ロピナビル/リトナビル(1,000/400/100mg1日2回)を併用した場合に、サキナビル/リトナビル(1,000/100mg1日2回)を投与した場合と比較して、リトナビルのAUC、Cmaxは減少したが、サキナビル、ロピナビルのAUC、Cmaxに影響はなかったとの報告がある。 |
チトクロームP450(CYP3A4)に対する競合による。 |
|
左記の薬剤の血中濃度が増加するおそれがある。 | チトクロームP450(CYP3A4)に対する競合による。 |
|
左記の薬剤の血中濃度が変化するおそれがある。併用する場合には、INRをモニタリングすることが望ましい。 | チトクロームP450(CYP3A4、CYP2C9)に対する競合による。 |
|
本剤の血中濃度が減少するおそれがある。併用する場合には本剤の血中濃度の減少による本剤の効果の減少に注意すること。 | 左記の薬剤はチトクロームP450(CYP3A4)を誘導する。 |
|
左記の薬剤の血中濃度を増加させるおそれがある。併用する場合には、左記の薬剤の治療濃度をモニタリングすることが望ましい。 | チトクロームP450(CYP2D6)に対する競合による。 |
| クラリスロマイシン |
本剤及びクラリスロマイシンのAUC、Cmaxが増加したとの報告がある。 腎機能障害のある患者は、クラリスロマイシンを減量すること。 30≦Ccr≦60mL/分:50%減量 Ccr<30mL/分:75%減量 |
チトクロームP450(CYP3A4)に対する競合による。 |
| エリスロマイシン | H I V感染患者において、サキナビル(1,200mg1日3回)とエリスロマイシン(250mg1日4回)を併用した場合に、サキナビルのAUCが99%、Cmaxが106%上昇したとの報告がある。 | チトクロームP450(CYP3A4)に対する競合による。 |
|
本剤の血中濃度が増加するおそれがある。 | チトクロームP450(CYP3A4)に対する競合による。 |
|
本剤のAUCを増加させたとの報告がある。 | チトクロームP450(CYP3A4)に対する競合による。 |
| リファブチン | 左記の薬剤の血中濃度が増加するおそれがある。 | チトクロームP450(CYP3A4)に対する競合による。 |
|
左記の薬剤の血中濃度が増加するおそれがある。併用する場合には、患者の状態(鎮静効果)に注意し、必要に応じて左記の薬剤の減量を考慮すること。 | チトクロームP450(CYP3A4)に対する競合による。 |
|
左記の薬剤の血中濃度が増加するおそれがある。併用する場合には、患者の状態を注意して観察すること。 | チトクロームP450(CYP3A4)に対する競合による。 |
| デキサメタゾン | 本剤の血中濃度を減少させるおそれがある。併用する場合には本剤の血中濃度の減少による本剤の効果の減少に注意すること。 | 左記の薬剤はチトクロームP450(CYP3A4)を誘導する。 |
| フルチカゾン ブデソニド |
低用量のリトナビルの使用により、経口吸入、経鼻投与された左記の薬剤の全身暴露症状(クッシング症候群等)が報告されている。 | チトクロームP450(CYP3A4)に対する競合による。 |
|
サキナビルメシル酸塩(600mg)を食事とともにラニチジン(150mg1日2回)と併用した場合に、食事のみの場合と比較して、サキナビルのAUCが67%、Cmaxが74%増加したとの報告がある。 | 機序不明 |
|
左記の薬剤の血中濃度が増加するおそれがある。併用時には、筋障害の症状(筋脱力感、筋痛、CK(CPK)の上昇等)に注意すること。 | チトクロームP450(CYP3 A4)に対する競合による。 |
|
左記の薬剤の血中濃度が増加するおそれがある。 | チトクロームP450(CYP3 A4)に対する競合による。 |
|
左記の薬剤の血中濃度が減少するおそれがある。併用する場合には、別の避妊方法を考慮すること。 | 機序不明 |
|
左記の薬剤の血中濃度が増加するおそれがある。併用する場合には、左記の薬剤の副作用(血圧低下、視覚障害等)の増加に注意すること。 | チトクロームP450(CYP3 A4)に対する競合による。 |
|
サキナビルメシル酸塩/リトナビル(1
,000/100mg1日2回)とオメプラゾール(40mg1日1回)を併用した場合に、サキナビルメシル酸塩/リトナビルのみの場合と比較して、サキナビルのAUC、Cmaxがそれぞれ82%、75%増加したとの報告がある。 併用する場合には、サキナビルの副作用発現に注意すること。 |
機序不明 |
| グレープフルーツジュース | サキナビルメシル酸塩(600m g)を1倍又は2倍濃縮のグレープフルーツジュースで単回投与した場合に、サキナビルのAUCがそれぞれ50%、100%増加したとの報告がある。 | チトクロームP450(CYP3 A4)に対する競合による。 |
| ニンニク成分含有製品 | 本剤の血中濃度が低下するおそれがあるので、本剤投与時は、ニンニク成分含有製品を摂取しないよう注意すること。サキナビル(1,200 mg1日3回)とニンニクカプセル(ニンニク約8gに相当する)を併用した場合に、サキナビルのAUCが51%、8時間後の平均トラフ値が49%、 Cmaxが54%減少したとの報告がある。 | 明確な機序は不明であるが、ニンニク成分により誘導された肝薬物代謝酵素(チトクロームP450)が本剤の代謝を促進し、クリアランスを上昇させるためと考えられている。 |
| セイヨウオトギリソウ(St. John’ sWort,セント・ジョーンズ・ワート)含有食品 | 本剤の代謝が促進され血中濃度が低下するおそれがあるので、本剤投与時はセイヨウオトギリソウ含有食品を摂取しないよう注意すること。 | セイヨウオトギリソウにより誘導された肝薬物代謝酵素(チトクロームP450)が本剤の代謝を促進し、クリアランスを上昇させるためと考えられている。 |
|
左記の薬剤の血中濃度が増加するおそれがある。 | チトクロームP450(CYP3 A4)に対する競合による。 |
|
左記の薬剤の血中濃度が増加するおそれがある。 | P-糖蛋白機能の阻害による。 |
注2)国内では外用剤のみ
4.副作用
国外における臨床第Ⅳ相試験(MaxCmin1試験)において、サキナビル/リトナビル(1,000mg/100mg)と少なくとも2剤の核酸系逆転写酵素阻害剤/非核酸系逆転写酵素阻害剤の併用群148例中104例(70.3%)に副作用が認められた。主な副作用は、下痢30件(20.3%)、悪心 26件(17.6%)、疲労15件(10.1%)、嘔吐14件(9.5%)、腹痛11件(7.4%)、鼓腸11件(7.4%)等であった。
〈参考:インビラーゼカプセルにおいて報告された国内の副作用〉
国内における承認時迄の調査及び使用成績調査309例注3)において、副作用は148例(47.9%)に認められた。主な副作用は、高脂血症21件(6.8%)、血中トリグリセリド上昇20件(6.5%)、肝機能異常20件(6.5%)、下痢17件(5.5%)、悪心17件(5.5%)、貧血11件(3.6%)、AST(GOT)上昇10件(3.2%)、ALT(GPT)上昇10件(3.2%)等であった。(第10回安全性定期報告時)
注3)国内における本薬のカプセル剤のデータ
(1)重大な副作用
次のような副作用があらわれた場合には、投与を中止するなど適切な処置を行うこと。
- 1)自殺企図(0.7%)、錯乱、幻覚(以上頻度不明a)):
- 自殺企図、錯乱、幻覚などがあらわれることがあるので、患者の状態を十分に観察すること。
- 2)痙攣、失調、多発性脊髄神経根炎、頭蓋内出血、脳出血、脳血管発作(以上頻度不明a)):
- 痙攣、失調、多発性脊髄神経根炎、死亡にいたる頭蓋内出血があらわれることがあるので、観察を十分に行うこと。
- 3)膵炎、腸管閉塞、腹水(以上頻度不明a)):
- 死亡にいたる膵炎や腸管閉塞、腹水などがあらわれることがあるので、定期的なアミラーゼ検査を行うなど、観察を十分に行うこと。
- 4)重度の肝機能障害、黄疸、肝炎、門脈圧亢進、硬化性胆管炎(以上頻度不明a)):
- 重度の肝機能障害、黄疸、門脈圧亢進、硬化性胆管炎があらわれることがあるので、定期的な肝機能検査を行うなど、観察を十分に行うこと。
- 5)高血糖(0.7%)、糖尿病(1.4%)、糖尿病の悪化(頻度不明a)):
- 糖尿病、糖尿病の悪化、高血糖があらわれ、その中には重篤な症例やケトアシドーシスを伴っていた症例の報告がある。このような症状があらわれた場合には、インスリンや血糖降下剤の投与等適切な処置を行うこと。
- 6)汎血球減少症、溶血性貧血、白血球減少症、血小板減少症(以上頻度不明a))、好中球減少症(0.7%):
- 汎血球減少症、溶血性貧血、好中球減少症、白血球減少、血小板減少症があらわれることがあるので、観察を十分に行うこと。
- 7)血栓性静脈炎、出血、末梢血管収縮(以上頻度不明a)):
- 血栓性静脈炎、出血、末梢血管収縮があらわれることがあるので、観察を十分に行うこと。
- 8)進行性多巣性白質脳症、灰白髄炎(以上頻度不明a)):
- 進行性多巣性白質脳症、灰白髄炎があらわれることがあるので、観察を十分に行うこと。
- 9)急性骨髄芽球性白血病、腫瘍(以上頻度不明a)):
- 急性骨髄芽球性白血病、腫瘍があらわれることがあるので、観察を十分に行うこと。
- 10)皮膚粘膜眼症候群(Stevens-Johnson症候群)(頻度不明a)):
- 皮膚粘膜眼症候群(Stevens-Johnson症候群)があらわれることがあるので、観察を十分に行うこと。
- 11)急性腎不全、腎結石症(以上頻度不明a)):
- 急性腎不全、腎結石症があらわれることがあるので、観察を十分に行うこと。
- 12)チアノーゼ、喀血(以上頻度不明a)):
- チアノーゼ、喀血があらわれることがあるので、観察を十分に行うこと。
- 13)無力症(2.0%)、多発性関節炎(頻度不明a)):
- 無力症、多発性関節炎があらわれることがあるので、観察を十分に行うこと。
(2)その他の副作用
次のような副作用があらわれた場合には、症状に応じて適切な処置を行うこと。
| 頻度不明a) | 2%以上b) | 2%未満c) | |
|---|---|---|---|
| 精神・神経 | 傾眠、会話障害、精神障害、知能低下、精神病、思考異常、神経過敏、多幸症、不安、失神、意識消失、異常感覚、健忘、構語障害、嗜眠、知覚過敏、反射減弱・亢進、不全麻痺、異常行動、ニューロパシー、下腿痙直、嗅覚障害、激越、うつ病、異常な夢、不眠症、感覚減退、振戦 | 末梢性ニューロパシー(2.7%)、味覚異常(2.7%)、頭痛(2.0%) | 浮動性めまい、性欲障害、易刺激性、錯感覚 |
| 消化器 | 耳下腺障害、胃痛、胃不快感、嚥下障害、血便排泄、歯痛、歯肉炎、食道炎、舌炎、唾液腺障害、直腸出血、排便回数増加、排便痛、歯の障害、変色便、メレナ、胃食道逆流性疾患、腹部不快感、肛門周囲瘙痒症、消化管潰瘍(食道・胃腸)、便失禁、口内炎(アフタ性を含む)、口唇炎 | 下痢(感染性を含む)(20.3%)、悪心(17.6%)、嘔吐(9.5%)、腹痛(7.4%)、鼓腸(7.4%)、上腹部痛(3.4%)、アミラーゼ増加(2.7%)、便秘(2.7%)、消化不良(2.0%)、腹部膨満(2.0%)、軟便(2.0%) | 口内乾燥、おくび、口唇乾燥、胃炎、胃腸炎(感染性、非感染性)、痔核、口腔内潰瘍形成 |
| 血液 | 微小出血、脾腫、リンパ球数減少、リンパ節症 | 貧血(3.4%) | ヘモグロビン減少 |
| 皮膚 | 毛髪変化、光線過敏性反応、紅斑、瘡瘡、色素沈着変化、脂漏性皮膚炎、蕁麻疹、水疱性皮疹、多汗症、脱毛症、爪の障害、斑状丘疹性皮疹、皮膚潰瘍、皮膚出血、皮膚障害、皮膚小結節、丘疹、瘙痒性皮疹、皮膚症候群、伝染性軟属腫、せつ、乾癬、皮下出血、皮膚乳頭腫、寝汗、乾皮症 | 皮膚乾燥(4.1%)、瘙痒(4.1%)、発疹(4.1%)、湿疹(3.4%) | 皮膚炎 |
| 抵抗機構 | 寄生虫感染、HIV消耗症候群、インフルエンザ、細菌・真菌感染、膿瘍、カポジ肉腫、蜂巣炎、単純ヘルペス、帯状疱疹、乳頭腫 | 毛包炎、カンジダ症 | |
| 肝臓 | 胆石症、肝腫大、肝脾腫大、γ-GTP増加 | ALP増加(3.4%)、 ALT(GPT)増加(2.7%)、高ビリルビン血症(2.7%)、AST(GOT)増加(2.0%) | LDH増加 |
| 内分泌・代謝 | 高K血症、低K血症、高Ca血症、低Ca血症、高Na血症、食欲障害、脱水、低血糖症、低P血症、高脂血症、甲状腺機能低下症、血中尿酸増加、血中甲状腺刺激ホルモン(TSH)増加 | リポジストロフィー(胸部、体幹部の脂肪の増加、末梢部の脂肪減少、野牛肩、クッシング様顔貌)(5.4%)d)、高トリグリセリド血症(2.0%)、食欲不振・減退(2.0%) | 血中コレステロール増加、低Na血症、低比重リポ蛋白コレステロール増加 |
| 呼吸器 | 呼吸障害、肺疾患、鼻出血、急性扁桃炎、喉頭炎、気管支炎、肺炎、鼻炎(アレルギー性を含む)、副鼻腔炎、上気道感染、喘息、咳嗽 | 呼吸困難、咽頭炎 | |
| 循環器 | 心拍障害、心弁膜障害、静脈拡張、低血圧、ほてり、心雑音 | 高血圧 | |
| 筋・骨格 | 組織変化、筋骨格障害、筋骨格痛、筋痛、顎痛、ミオパシー、四肢痛、 CK(CPK)増加、関節炎、背部痛、筋骨格硬直 | 関節痛、筋痙縮 | |
| 感覚器 | 眼球乾燥、眼瞼炎、霰粒腫、眼刺激、結膜炎、耳痛、聴力低下、耳鳴、耳圧迫感、耳炎、サイトメガロウイルス性脈絡網膜炎、眼乾燥症候群 | 視覚障害 | |
| 腎臓 | 尿路感染、尿路出血、排尿異常、腎仙痛 | 夜間頻尿、血中クレアチニン増加 | |
| 生殖器 | 骨盤痛、腟分泌物、勃起不全、前立腺肥大、精巣上体炎、月経障害、不規則月経、陰茎障害 | ||
| その他 | 戦慄、顔面痛、粘膜障害、浮腫、疼痛、口渇、胸痛、倦怠感 | 疲労(10.1%)、発熱(2.0%)、体重減少(2.0%) | 過敏症、体重増加 |
a)国外における臨床第Ⅳ相試験(MaxCmin1試験)において報告されなかったが、サキナビル製剤(サキナビルメシル酸塩、サキナビル)の国外添付文書に記載のある副作用又は国内において報告されたサキナビルメシル酸塩カプセルの副作用
b)国外における臨床第Ⅳ相試験(MaxCmin1試験)において2%以上の頻度で発現した副作用
c)国外における臨床第Ⅳ相試験(MaxCmin1試験)において2%未満の発現頻度であったが、サキナビル製剤(サキナビルメシル酸塩、サキナビル)の国外添付文書に記載のある副作用
d)臨床症状及び臨床検査値(血中脂質、血糖)に注意し、代謝異常が認められた場合には適切な処置を行うこと。
5.高齢者への投与
高齢者へ投与する場合には、以下の理由から、患者の状態を観察しながら慎重に投与すること。
- 本剤は、主として肝臓で代謝されるが、高齢者では肝機能が低下していることが多いため高い血中濃度が持続するおそれがある。
- 本剤は、血漿蛋白結合率が高いが、高齢者では血漿アルブミンが減少していることが多いため、遊離の薬物の血中濃度が高くなるおそれがある。
6.妊婦、産婦、授乳婦等への投与
- 妊婦又は妊娠している可能性のある婦人には、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。[妊娠中の投与に関する安全性は確立していない。]
- 授乳婦に投与する場合には、授乳を避けさせること。[本剤の乳汁中への移行については不明である。]
7.小児等への投与
低出生体重児、新生児、乳児、幼児又は小児に対する安全性は確立していない。[使用経験が少ない。]
8.過量投与
過量投与が明白又は疑われた場合には、できるだけ速やかに催吐剤の投与又は胃洗浄等の適切な処置を行うこと。
【薬物動態】
〈日本人における成績〉
血漿中濃度
HIV感染患者(n=6)にサキナビルメシル酸塩(サキナビルとして1回600mg)を1日3回反復経口投与※(測定時点:投与開始4~12週)したときの薬物動態学的パラメータは表1のとおりであった。
| Tmax (hr) |
Cmax (ng/mL) |
AUC0-8 (ng・hr/mL) |
|
|---|---|---|---|
| 最小値 | 2.00 | 94.9 | 401.1 |
| 平均値 | 3.92 | 211.0 | 855.1 |
| 最大値 | 6.00 | 595.0 | 2035.7 |
※本剤の承認された用法・用量はサキナビル1,000mg/リトナビル100mgを1日2回投与である。
〈外国人における成績(参考)〉1)
1.血漿中濃度
HIV感染患者にサキナビルメシル酸塩又はサキナビル単独で1日3回投与時又はそれぞれのリトナビルとの併用で1日2回投与時※の定常状態における薬物動態パラメータを表2に示した。
サキナビルはP-糖蛋白(MDR1)の基質となることが知られている。
| 投与方法 | N | AUC0-24 (ng・hr/mL) |
Cmin (ng/mL) |
|---|---|---|---|
| サキナビルメシル酸塩600mg1日3回投与(算術平均値) | 10 | 866♭ | 79 |
| サキナビル1,200mg1日3回投与(算術平均値) | 31 | 21747 | 216 |
| サキナビルメシル酸塩1,000mg+リトナビル100mg1日2回投与(幾何平均値) | 24 | 29214 | 371 |
| サキナビル1,000mg+リトナビル100mg1日2回投与(幾何平均値) | 24 | 38170 | 433 |
サキナビルメシル酸塩の投与量はサキナビル換算量 ♭:AUC0-8
※本剤の承認された用法・用量はサキナビル1,000mg/リトナビル100mgを1日2回投与である。
2.食事の影響
HIV感染患者(n=22)に1日2回、サキナビルとして1,000mgのサキナビルメシル酸塩と100mgのリトナビルを3回投与後の絶食および高脂肪食(脂肪46g、1,091kcal)時のAUC0-12はそれぞれ10,320ng・h/mLおよび34,926ng・h/mLであった。
| 投与方法 | N | AUC0-24 (ng・hr/mL) |
Cmin (ng/mL) |
|---|---|---|---|
| サキナビルメシル酸塩1,000mg+リトナビル100mg1日2回投与 (絶食時投与、幾何平均値) |
22 | 20640 | 313 |
| サキナビルメシル酸塩1,000mg+リトナビル100mg1日2回投与 (高脂肪食時投与、幾何平均値) |
22 | 69852 | 1179 |
3.成人における体内分布
サキナビルとして12mg静脈内投与(n=8)後の定常状態の分布容積は700L(変動係数39%)であり、サキナビルが組織へ移行することが示唆されている。濃度範囲15~700ng/mLにおけるサキナビルの血漿蛋白結合率は、ほぼ98%であった。サキナビルとして1回600mgを1日3回投与した患者2名において、脳脊髄液中濃度は対応する血漿中濃度と比較し無視できる程度であった。
(参考)動物実験の結果
動物実験(ラット)における14C-サキナビル単回静脈内投与後(2.25mg/kg)の全身オートラジオグラフィーにおいて、21日目においても放射能の眼ぶどう膜への残留が認められた。マーモセットにおける12ヵ月間反復経口投与試験(3,000mg/kg/日)、イヌにおける4週間の反復経口投与試験(700mg/kg/日)において、眼底検査、病理組織学的検査、一般症状、神経学的検査で、メラニン変性による毒性の発現は認められていない。
4.成人における代謝及び排泄
ヒト肝臓ミクロソームを用いたin vitro試験で、サキナビルはチトクロームP450により代謝され、特に肝臓における代謝の90%以上がアイソザイムCYP3A4に因ることが示されている。サキナビルは速やかに不活性なモノ‐及びジ‐水酸化体へ代謝される。14C-サキナビルメシル酸塩(サキナビルとして600mg)を単回経口投与した健康成人(n=8)において、投与後5日までに投与放射能の88%及び1%が、それぞれ糞及び尿中へ排泄された。別の被験者(n=4)に14C-サキナビル10.5mgを単回静脈内投与した際、投与後5日までに投与放射能の79%及び3%が、それぞれ糞及び尿中へ排泄された。14C-サキナビルメシル酸塩を経口投与後、血漿中放射能の13%が未変化体であり残りは代謝物であった。静脈内投与後では、血漿中放射能の66%が未変化体、残りが代謝物であり、サキナビルが著しく初回通過代謝を受けることが示唆された。サキナビルの全身クリアランスは速やかで、6、36、72mg静脈内投与後の値は1.14L/h/kg(変動係数12%)であった。平均滞留時間は7時間(n=8)であった。
5.肝又は腎機能障害患者
肝又は腎機能障害(特に重度の)患者におけるサキナビルの薬物動態は検討されていない。なお、サキナビルの尿中排泄率は1%である。
6.性・人種・年齢
インビラーゼ500mg錠と200mgカプセルのリトナビル100mg併用下における同等性試験においてサキナビルのAUC及びCmaxについて性差が認められた。男性と比較して女性においてAUC及びCmaxがそれぞれ56%及び26%の高値を示した。しかし、サキナビル1,000mgにリトナビル100mgを併用した場合に、性別による安全性および有効性の差異は見られなかった。
なお、サキナビルの薬物動態の人種間差については明らかとはなっていない。また、小児及び65歳以上の高齢者における薬物動態については検討されていない。
7.薬物相互作用2-5)
サキナビルは肝臓における代謝の90%がCYP3A4により代謝される。更にP-糖蛋白(MDR1)の基質となることが知られている。したがって、これらに影響を及ぼす薬物は、サキナビルの体内動態に影響を及ぼす可能性がある。また、併用されるリトナビルはCYP3A4を阻害することから、この酵素で代謝される薬物の体内動態に影響を及ぼす可能性がある。
HIV感染患者(n=32)において、インビラーゼ1,000mgとリトナビル100mgを1日2回投与時にエファビレンツを併用したときのサキナビル及びエファビレンツの濃度には臨床的に有意な変化は見られなかった。
HIV感染患者(n=20)にサキナビル1,600mgとリトナビル200mgを1日1回投与時にリファンピシン併用によりサキナビルのAUCは50%低下した。
なおその他、報告されているサキナビルと併用薬との相互作用を表3、表4に示した。
| 併用薬 | サキナビル投与量 | N | サキナビルの薬物動態(%Change) | |
|---|---|---|---|---|
| AUC(95%CI) | Cmax(95%CI) | |||
| クラリスロマイシン500mg 1日2回7日間 |
1,200mg1日3回 7日間 |
12V | ↑177% (108-269%) |
↑187% (105-300%) |
| エファビレンツ600mg | 1,200mg1日3回 | 13V | ↓62% | ↓50% |
| インジナビル800mg 1日3回2日間 |
1,200mg単回投与 | 6V | ↑364% (190-644%) |
↑299% (138-568%) |
| ケトコナゾール400mg 1日1回 |
1,200mg1日3回 | 12V | ↑190% | ↑171% |
| ネルフィナビル750mg 4日間 |
1,200mg単回投与 | 14P | ↑392% (271-553%) |
↑179% (105-280%) |
| リファブチン300mg 1日1回 |
1,200mg1日3回 | 14P | ↓47% | ↓39% |
| リファンピシン600mg 1日1回 |
1,200mg1日3回 14日間 |
14V | ↓70% | ↓65% |
| リトナビル100mg 1日2回 |
1,000mg1日2回 (対照群:サキナビル1,200mg 1日3回 n=33) |
24P | ↑176% | ↑153% |
| リトナビル400mg 1日2回14日間 |
400mg1日2回14日間 (対照群:サキナビル1,200mg 1日3回 n=33) |
8V | ↑121% (7-359%) |
↑64% |
| ロピナビル/リトナビル 400/100mg 1日2回15日間 |
800mg1日2回10日間 (対照群:サキナビル1,200mg 1日3回5日間) |
14V | ↑9.62倍 (8.05、1.49)$ |
↑6.34倍 (5.32、7.55)$ |
| ロピナビル/リトナビル 400/100mg 1日2回20日間 |
1,200mg1日2回10日間 (対照群:サキナビル1,200mg 1日3回 n=33) |
10V | ↑9.91倍 (8.28、11.86)$ |
↑6.44倍 (5.59、7.41)$ |
| 以下はサキナビルメシル酸塩の結果 | ||||
| リファブチン 150mg3日間又は 300mg7日間 |
400mg1日2回 400mgリトナビル 1日2回併用 |
24P | ↑19% | ↑39% |
| リトナビル400mg 1日2回(定常状態時) |
400mg1日2回(定常状態時) (対照群:サキナビルメシル酸塩600mg 1日3回 n=114) |
7P | ↑1,587% (808-3,034%) |
↑1,277% (577-2,702%) |
| リトナビル100mg 1日2回 |
1,000mg1日2回 (対照群:サキナビルメシル酸塩600mg 1日3回 n=114) |
24P | ↑1,124% | ↑1,325% |
$:90%信頼区間
V:健康成人を対象とした試験
P:HIV感染患者を対象とした試験
| 併用薬 | サキナビル又は リトナビル併用サキナビル投与量 |
N |
併用薬の薬物動態 (% Change) |
|
|---|---|---|---|---|
| AUC(95%CI) | Cmax(95%CI) | |||
| クラリスロマイシン 500mg 1日2回7日間 |
1,200mg1日3回7日間 | 12V | クラリスロマイシン ↑45% (17-81%) 14-OHクラリスロマイシン ↓24% (5-40%) |
クラリスロマイシン ↑39% (10-76%) 14-OHクラリスロマイシン ↓34% (14-50%) |
| ミダゾラム7.5mg 経口単回投与 |
1,200mg1日3回5日間 | 6V | ↑514% | ↑235% |
| ケトコナゾール400mg 1日1回投与 |
1,200mg1日3回 | 12V | ←→ | ←→ |
| エンフューヴィルタイド#90mg 1日2回皮下投与 7日間 |
1,000/100mg1日2回 | 12P | ←→ | ←→ |
| ネルフィナビル750mg 単回投与 |
1,200mg1日3回4日間 | 14P | ↑18% (5-33%) |
←→ |
| リファブチン300mg 1日1回投与 |
1,200mg1日3回 | 14P | ↑44% | ↑45% |
| リトナビル400mg 1日2回14日間 |
400mg1日2回14日間 | 8V | ←→ | ←→ |
| シルデナフィル100mg 単回投与 |
1,200mg1日3回8日間 | 27V | ↑210% (150-300%) |
↑140% (80-230%) |
| エファビレンツ600mg | 1,200mg1日3回 | 13V | ↓12% | ↓13% |
| ジゴキシン0.5mg単回投与 | 1,000/100mg1日2回16日間 | 16V | ↑49%(32-69%)Φ | ↑27%(5-54%)Φ |
| リファブチン150mg1日4回投与 | 1,000/100mg1日2回 | 11V | ↑60%Эл(43-79%)Φ ←→§(-10to13%)Φ |
↑111%Эл(75-153%)Φ ↑68%§(38-105%)Φ |
V:健康成人を対象とした試験
P:HIV感染患者を対象とした試験
#:国内未発売
Φ:90%信頼区間
Э:活性物質(リファブチン+25-O-desacetyl体)のAUC0-96及びCmaxによる比較
л:リファブチン1日1回150mg投与との比較
§:リファブチンのAUC0-96及びCmaxによる比較
(参考)動物実験の結果
- 1.イヌにおける反復併用毒性試験
- 動物実験(イヌ)におけるサキナビル(200mg/kg/日)とリトナビル(5及び25mg/kg/日)との4週間反復併用経口毒性試験において、サキナビルのAUCはリトナビル5mg/kg/日との併用で約10倍、リトナビル25mg/kg/日との併用で約15倍に上昇した。これらの値はサキナビルメシル酸塩1,000mg(サキナビル換算)とリトナビル100mgを1日2回投与した患者でのAUCの3~5倍であった。しかし、併用投与時における忍容性は良好であり、毒性の増強は認められなかった。
- 2.トキシコキネティックス試験
- マウス、ラット、マーモセット及びイヌを用いた毒性試験で、それぞれ臨床用量(1,000mg1日2回=2,000mg/日;33.3mg/kg/日)の約150倍、75倍、90倍及び21倍の用量まで反復経口投与がなされた。その際の各動物種におけるAUCは、サキナビルメシル酸塩1,000mg(サキナビル換算)とリトナビル100mgを1日2回投与した患者でのAUCの約0.5~6倍と算出されたが、いずれの動物種においてもほとんど毒性兆候は認められなかった。1例のイヌにおいて併用患者の22倍に相当するAUCが認められ、この場合には病理所見を伴う軽度の肝毒性が観察された。
8.心電図に対する影響
18~55歳までの健康男性及び女性を対象(N=59)とし、陽性対照薬にモキシフロキサシン400mgを用いた4-way crossoverの二重盲検試験で、インビラーゼ/リトナビル1,000/100mgを1日2回及び1,500/100mgを1日2回投与時のQT間隔に与える影響を検討した。 プラセボ群との間における投与前ベースライン補正を行った陽性対照群及びインビラーゼ/リトナビル投与群の試験特異的な補正式を用いて算出したQTc間隔(QTcS間隔)の変化(ddQTcS間隔)及び95%信頼区間(片側)を表に示した。
本試験において、QTc間隔が500msecを超えた被験者はいなかった。
PR間隔が200msecを超える被験者はインビラーゼ/リトナビルの1,000/100mg、1,500/100mg投与群においてそれぞれ40%及び47%認められ、PR間隔の変化の平均値の最大値はそれぞれ25msecと34msecであった。
なお、健康成人にインビラーゼ/リトナビル1,000/100mgを1日2回投与した際の投与3日目のサキナビルのCmax(平均値)は、HIV患者集団における定常状態のCmaxの約3~4倍であった。
インビラーゼ/リトナビル1,000/100mgまたは1,500/100mg1日2回3日間投与後及びモキシフロキサシン投与後におけるddQTcS(msec)†の平均値の最大値
| 投与量 | 投与後時間 | ddQTcS の平均値 の最大値 |
標準誤差 | ddQTcS 上側95% 信頼区間 |
|---|---|---|---|---|
| インビラーゼ/リトナビル 1,000/100mg1日2回 |
12時間 | 18.86 | 1.91 | 22.01 |
| インビラーゼ/リトナビル 1,500/100mg1日2回 |
20時間 | 30.22 | 1.91 | 33.36 |
| モキシフロキサシン^ | 4時間 | 12.18 | 1.93 | 15.36 |
†:ベースラインからの変化をプラセボ投与時の変化で補正したときの平均QTcSの最大値
^ :3日目に400mgを投与
【臨床成績】
〈外国人における成績〉
HIV感染成人患者(148例)にサキナビル/リトナビル1,000/100mg1日2回投与に、更に2つの逆転写酵素阻害剤を併用して、臨床第Ⅳ相試験(MaxCmin1試験、デンマーク、他12カ国)がおこなわれた。
その結果、血漿中HIV-RNAが400copies/mL以下の患者は、投与前で38%、48週では69%であった。48週でのCD4リンパ球数の増加は85cells/μL(中央値)であった。
【薬効薬理】
1.作用機序6)
HIVプロテアーゼは、HIVに感染した細胞においてウイルスの前駆体ポリ蛋白質を切断し、ウイルス酵素及び構造蛋白質を生じさせる。この過程を経てウイルスは成熟し感染性を示すようになる。サキナビルはHIV-1及びHIV-2プロテアーゼの活性を阻害するペプチド様合成基質アナログであり、HIVプロテアーゼによる前駆体ポリ蛋白質の切断を阻害することで感染性をもつウイルスの産生を阻害する。サキナビルの阻害作用はHIVプロテアーゼに選択的であり、ヒトのプロテアーゼ(レニン、カテプシンD、エラスターゼ、コラゲナーゼ等)活性には阻害作用を示さない。
2.抗ウイルス作用7)
ヒトリンパ芽球系細胞株及び単球系細胞株、末梢血リンパ球におけるサキナビルのin vitro抗ウイルス作用を検討した。サキナビルは各種HIV-1株(GB8、RF、MN 等)あるいはHIV-2ROD株を急性感染させた細胞においてHIVの増殖を阻害し、IC50値(50%阻害濃度)は1~30nMの範囲であった。また、HIV-1LAV株を慢性感染させたヒト前単球系細胞株(U1)において、サキナビルは100nM以上の濃度でウイルス粒子の成熟化を阻害した。更にHIV-1GB8株を感染させたヒトTリンパ芽球系細胞株(CEM)の培養系において、サキナビルと核酸系逆転写酵素阻害剤ジドブジン(AZT)あるいはザルシタビン(ddC)との2剤ないし3剤の併用投与は相乗的な増殖阻害効果を示した。
3.薬剤耐性8-11)
in vitroで作成したサキナビル耐性HIV分離株のプロテアーゼには、48番目及び90番目のアミノ酸部位に置換突然変異が認められた(48番目はグリシンからバリンヘの置換:G48V、90番目はロイシンからメチオニンヘ置換:L90M)。ヒトにおいても、サキナビル投与患者由来のHIV分離株のプロテアーゼで同様の突然変異が認められた。
サキナビル単独、サキナビル/AZT(ジドブジン)併用又はサキナビル/AZT/ddC(ザルシタビン)併用による臨床試験におけるHIVプロテアーゼの突然変異(G48VとL90M)の発現率は、臨床第Ⅰ/Ⅱ相試験(16~74週間投与)では36%(31/85例)、また、臨床第Ⅲ相試験では、20~29週間投与での発現率は20%(16/81例)、40~72週間投与での発現率は32%(24/75例)であった。このG48VとL90Mの突然変異は、サキナビルに対する感受性をわずかに低下させる(この変異によるIC50値の上昇は、概ね10倍以下であった)。
リトナビルやインジナビルに耐性を示す患者26例を含むサキナビル未治療患者32例におけるサキナビル/リトナビル(1,000/100mg 1日2回投与)/エファビレンツ/核酸系逆転写酵素阻害剤との併用投与試験において、32例中19例がベースライン時点でサキナビルに感受性があった。24週目の時点で、投与開始時にサキナビルに感受性があった患者の58%、サキナビルに対する感受性が低下していた患者(IC50値の上昇は10倍以上であった)の25%でHIV-RNA量が50copies/mL以下となった。
4.交差耐性10,12-15)
HIVプロテアーゼ阻害剤間における交差耐性については、サキナビルを核酸系逆転写酵素阻害剤と併用、又は併用せずに20~147週間投与した患者から分離したサキナビル耐性HIV株の18%が他のHIVプロテアーゼ阻害剤(インジナビル、リトナビル、ネルフィナビル、アンプレナビル)に対する幅広い交差耐性を示し、55%が他のプロテアーゼ阻害剤の少なくとも1種類に対して耐性を示した。
一方、リトナビル、ネルフィナビル、アンプレナビルのいずれかに顕著な耐性を示す分離HIV株は、サキナビルに対しては耐性を示さなかった。
核酸系逆転写酵素阻害剤との交差耐性に関しては、AZT耐性HIV分離株がサキナビルに感受性をもつことがin vitroで示されている。
【有効成分に関する理化学的知見】
- 一般名
- サキナビルメシル酸塩(Saquinavir Mesilate)(JAN)
- 化学名
- (-)-cis-N-tert-butyldecahydro-2-{(2R, 3S)-2-hydroxy-4-phenyl-3-{[N-(2-quinolylcarbonyl)-L-asparaginyl]amino}butyl}-(3S,4aS,8aS)-isoquinoline-3-carboxamide monomethanesulfonate
- 構造式
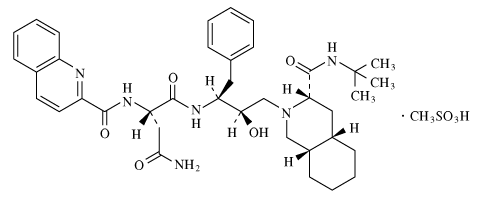
- 分子式
- C38H50N6O5・CH3SO3H
- 分子量
- 766.95
- 性状
- 白色の粉末
- 旋光度
- [α]20436:-66.8°~-69.6°(水分を補正したもの0.25g、メタノール、50mL)
【承認条件】
- 実施中の臨床試験、あるいは市販後の使用において、重篤な有害事象が発生した際には速やかに報告を行うこと。
- 実施中の臨床試験については、プロトコールを遵守し、定期的(3ヶ月に1回程度を目途)に試験成績を報告し、試験終了次第、可及的速やかに試験成績、解析結果を提出すること。
-
今後、再審査期間の終了までは、国内で使用される症例に関しては、可能な限り全投与症例を市販後調査の対象とし、臨床効果、副作用、薬物相互作用等に関してデータの収集を行い、再審査の申請資料として提出すること。
なお、データの収集においては、特に、本剤と他のHIVプロテアーゼ阻害剤との併用による相互作用について十分な注意が必要であることに留意すること。 - 市販後、本剤の使用実態について詳細に調査を行い、他剤との併用における本剤の安全性、有効性に関する情報収集を実施し、定期的に報告すること。
- 治療にあたっては、本剤は現在我が国における臨床試験が行われており、薬剤に関する科学的なデータを収集中であること等、患者に十分な説明を行い、インフォームド・コンセントを得るように医師に対して要請すること。
【包装】
インビラーゼカプセル200mg:100カプセル(バラ)
インビラーゼ錠500mg:120錠(バラ)
【主要文献】
- 米国添付文書
- Lee CGL, et al.:Biochemistry 37(11) :3594, 1998
- Wacher VJ, et al.:J Pharm Sci 87(11):1322, 1998
- Kim AE, et al.:J Pharmacol Exp Ther 286(3) :1439, 1998
- Picketty C, et al.:AIDS 13(11):F71, 1999
- Roberts NA, et al.:Science 248 :358, 1990
- Craig JC, et al.:Antivir Chem Chemother 5(6):380, 1994
- Jacobsen H, et al.:Virology 206 :527, 1995
- Race E, et al.:AIDS 12 (12):1465, 1998
- Craig C, et al.:AIDS 12 (13):1611, 1998
- Piketty C, et al.:AIDS 14 (5):626, 2000
- Molla A, et al.:Nat Med 2 (7):760, 1996
- Tisdale M, et al.:Clin Drug Invest 20 (4):267, 2000
- Patick AK, et al.:Antimicrob Agents Chemother 42 (10):2637, 1998
- Johnson VA, et al.:J Infect Dis 166 :1143, 1992
【文献請求先】
中外製薬株式会社 医薬情報センター
〒103-8324 東京都中央区日本橋室町2-1-1
電話:0120-189706
Fax:0120-189705
- 製造販売元
- 中外製薬株式会社
- 東京都中央区日本橋室町2-1-1
| おくすりガイド|
おくすりガイド|



 Page Top
Page Top