
| 商品名: | レクシヴァ錠700 |
|---|---|
| 一般名: | ホスアンプレナビル |
| 略称 : | FPV |
ここで提供している添付文書情報は、2010年5月18日現在の各医薬品の添付文書を基に作成したものです。書式等については、実際の添付文書と異なるところがあります。添付文書情報は随時更新されます。ご使用の際は、必ず最新の添付文書をご覧下さい。
また、記載されている内容には、専門的な情報が含まれています。文書内の、
この色の文字をクリックすると、別ウィンドウに読み方のアドバイスが表示されます。
この色の文字をクリックすると、別ウィンドウに重大な副作用の解説が表示されます。
この色の文字をクリックすると、別ウィンドウに副作用の症状とその類似語、定義の解説が表示されます。
記載されている情報をご覧になり、疑問などを持たれた場合は、医師・薬剤師にご相談ください。
このページを開いた時に目次が自動的に表示されなかったときは、ここをクリックしてください。
抗ウイルス化学療法剤

ホスアンプレナビルカルシウム水和物錠
2013年1月改訂(第11版)
日本標準商品分類番号:87625
規制区分:劇薬、処方せん医薬品
(注意-医師等の処方せんにより使用すること)
貯法:室温保存
使用期限:包装に表示
| 承認番号 | 21600AMZ00652 |
|---|---|
| 薬価収載 | 2005年1月 |
| 販売開始 | 2005年1月 |
| 国際誕生 | 2003年10月 |
| 成分・含量 | 1錠中にホスアンプレナビルカルシウム水和物をホスアンプレナビルとして700mg含有する。 |
|---|---|
| 添加物 | 結晶セルロース、クロスカルメロースナトリウム、ポビドン、ステアリン酸マグネシウム、軽質無水ケイ酸、ヒプロメロース、酸化チタン、トリアセチン、三二酸化鉄 |
本剤は淡紅白色のフィルムコート錠で、識別コード及び形状は以下のとおりである。
| 販売名 | 識別コード | 表 | 裏 | 側面 | 質量 |
|---|---|---|---|---|---|
| レクシヴァ錠700 | GXLL7 |  長径:20.5mm 短径:9.5mm |
 |
 厚さ:7.4mm |
1174mg |
HIV感染症
通常、成人には以下の用法・用量に従い経口投与する。投与に際しては、必ず他の抗HIV薬と併用すること。
1.抗HIV薬の治療経験がない患者
2.HIVプロテアーゼ阻害剤の投与経験がある患者
本剤の活性代謝物であるアンプレナビルは、主としてCYP3A4で代謝される。また、アンプレナビルはCYP3A4の阻害作用を有する。
| 薬剤名等 | 臨床症状・措置方法 | 機序・危険因子 |
|---|---|---|
| 治療域が狭くCYP3A4で代謝される薬剤 | アンプレナビルとこれら薬剤はCYP3A4で代謝されるため、併用により代謝が競合的に阻害される。 | |
|
これら薬剤の血中濃度が上昇し、不整脈等の重篤な又は生命に危険を及ぼすような事象が起こる可能性がある。 | |
|
ベプリジル塩酸塩水和物の血中濃度が上昇し、生命に危険を及ぼす不整脈が起こる可能性がある。 | |
|
これら薬剤の血中濃度が上昇し、末梢血管攣縮、虚血等の重篤な又は生命に危険を及ぼすような事象が起こる可能性がある。 | |
|
これら薬剤の血中濃度が上昇し、過度の鎮静や呼吸抑制等の重篤な又は生命に危険を及ぼすような事象が起こる可能性がある。 | |
|
バルデナフィル塩酸塩水和物の血中濃度が上昇し、バルデナフィル塩酸塩水和物に関連する事象(低血圧、失神、視覚障害、持続勃起症等)の発現が増加する可能性がある。 | |
|
リファンピシンはアンプレナビルのCmin及びAUCをそれぞれ92%及び82%低下させるため、本剤の作用が減弱する。 | リファンピシンはCYP3A4の強力な誘導剤であるため、アンプレナビルの代謝が促進される。 |
| 薬剤名等 | 臨床症状・措置方法 | 機序・危険因子 |
|---|---|---|
| エファビレンツ | 本剤1400mg/リトナビル200mg1日1回とエファビレンツ600mg1日1回を併用した場合、アンプレナビルのAUCは13%、Cminは36%低下したが、リトナビルを300mgに増量すると、アンプレナビルの血中濃度は維持された。また、本剤700mg/リトナビル100mgの1日2回投与とエファビレンツ600mg1日1回を併用した場合、アンプレナビルの血中濃度に著しい変化はなかった。 | これら薬剤はCYP3A4を誘導するため、本剤の代謝が促進される。 |
| ネビラピン | 本剤1400mg1日2回とネビラピン200mg1日2回を併用した場合、アンプレナビルのCmax、AUC、Cminはそれぞれ25%、33%、35%低下し、ネビラピンのCmax、AUC、Cminはそれぞれ25%、29%、34%上昇した。 また、本剤700mg/リトナビル100mg1日2回とネビラピン200mg1日2回を併用した場合、アンプレナビルのAUC及びCminはそれぞれ11%、19%低下し、ネビラピンのCmax、AUC、Cminはそれぞれ13%、14%、22%上昇した。本剤700mg/リトナビル100mg1日2回とネビラピン200mg1日2回を併用する場合には、用量を調節する必要はない。 なお、本剤/リトナビル1日1回投与におけるネビラピンとの併用試験は実施されていない。 |
|
| デラビルジン | アンプレナビルのCmax、AUC、Cminはそれぞれ40%、130%、125%上昇した。一方、デラビルジンのCmax、AUC、Cminはそれぞれ47%、61%、88%低下し、デラビルジンの効果が減弱する可能性がある。 なお、デラビルジン併用時の推奨用量は確立していない。 |
アンプレナビルとこれら薬剤はCYP3A4で代謝されるため、併用により代謝が競合的に阻害される。 |
| インジナビル | アンプレナビルのCmax、AUC、Cminはそれぞれ18%、33%、25%上昇し、インジナビルのCmax、AUC、Cminはそれぞれ22%、38%、27%低下した。 なお、本剤及びリトナビルとインジナビルとの併用における推奨用量は確立していない。 |
|
| サキナビル | アンプレナビルのCmax、AUC、Cminはそれぞれ37%、32%、14%低下し、サキナビルのCmaxは21%上昇し、AUC及びCminはそれぞれ19%、48%低下した。 本剤及びリトナビルとサキナビルとの併用における推奨用量は確立していない。 |
|
| ネルフィナビル | アンプレナビルのCmaxは14%低下し、Cminは189%上昇し、ネルフィナビルのCmax、AUC、Cminはそれぞれ12%、15%、14%上昇した。 本剤及びリトナビルとネルフィナビルとの併用における推奨用量は確立していない。 |
|
| アタザナビル | 本剤700mg/リトナビル100mg1日2回とアタザナビル300mg1日1回を併用した場合、アタザナビルのCmax、AUCはそれぞれ24%、22%低下した。 なお、本剤及びリトナビルとアタザナビルとの併用における推奨用量は確立していない。 |
|
| ロピナビル・リトナビル配合剤 | 本剤700mg/リトナビル100mg1日2回とロピナビル・リトナビル(400mg・100mg)1日2回を併用した場合、アンプレナビルのCmax、AUC、Cminはそれぞれ58%、63%、65%低下し、ロピナビルのCmax、AUC、Cminはそれぞれ30%、37%、52%上昇した。 また、本剤1400mg1日2回とロピナビル・リトナビル(533mg・133mg)1日2回を併用した場合、アンプレナビルのCmax、AUC、Cminはそれぞれ13%、26%、42%低下した。 なお、本剤及びリトナビルとロピナビル・リトナビルとの併用における推奨用量は確立していない。 |
|
| リファブチン | アンプレナビルは、リファブチンのAUCを193%上昇させるため、本剤とリファブチンを併用する場合には、リファブチンの投与量を少なくとも半量に減量し、また、本剤/リトナビルとリファブチンを併用する場合には、リファブチンの投与量を少なくとも1/4に減量し、患者の臨床症状等を十分に観察すること。 | |
| リドカイン(全身投与) アミオダロン塩酸塩 キニジン硫酸塩水和物 三環系抗うつ剤 シクロスポリン タクロリムス rapamycin(国内未発売) |
これら薬剤の血中濃度が上昇する可能性があるので、血中濃度のモニタリングを行うことが望ましい。 | |
| ワルファリン | ワルファリンの血中濃度が上昇する可能性があるので、血液凝固能検査のモニタリングを行うことが望ましい。 | |
|
これら薬剤の血中濃度が上昇し、作用が増強する可能性がある。 | アンプレナビルとこれら薬剤はCYP3A4で代謝されるため、併用により代謝が競合的に阻害される。 |
| ジアゼパム フルラゼパム アルプラゾラム クロラゼプ酸二カリウム |
これら薬剤の血中濃度が上昇し、作用が増強する可能性がある。 | |
| シンバスタチン アトルバスタチン lovastatin(国内未発売) |
これら薬剤の血中濃度が上昇し、ミオパシー及び横紋筋融解症を起こす可能性がある。本剤700mg/リトナビル100mg1日2回とアトルバスタチン10mg1日1回を併用した場合、アトルバスタチンのCmax、AUC、Cmin はそれぞれ184%、153%、73%上昇した。本剤1400mg1日2回とアトルバスタチン10mg1日1回を併用した場合、アンプレナビルのCmax、AUC、Cminはそれぞれ18%、27%、12%低下した。一方、アトルバスタチンのCmax、AUCはそれぞれ304%、130%上昇し、Cminは10%低下した。 本剤と20mg/日以上のアトルバスタチンを併用する場合は、アトルバスタチンの副作用の発現に注意すること。なお、プラバスタチンやフルバスタチンの代謝にはCYP3A4は関与していないため、HMG-CoA還元酵素阻害剤を併用する場合にはプラバスタチンやフルバスタチンが推奨される。 |
|
| シルデナフィルクエン酸塩 タダラフィル |
シルデナフィルクエン酸塩、タダラフィルの血中濃度が上昇し、これら薬剤に関連する事象(低血圧、失神、視覚障害、持続勃起症等)の発現が増加する可能性がある。よって、併用する場合には、これら薬剤の減量を考慮するとともに、有害事象のモニタリングを行うなど注意すること。 | |
| ケトコナゾール(経口剤国内未発売) イトラコナゾール |
これら薬剤の血中濃度を上昇させる可能性がある。 特に、高用量のケトコナゾール、イトラコナゾール(>200mg/日)の投与は有益性が危険性を上回ると判断される場合のみ、十分な観察のもとで投与すること。 |
|
| エリスロマイシン クラリスロマイシン |
これら薬剤の血中濃度を上昇させる可能性がある。特に、リトナビルはクラリスロマイシンの血中濃度を上昇させるため、腎障害患者において本剤及びリトナビルとクラリスロマイシンを併用する場合は、クラリスロマイシンの用量を減量すべきである。 | |
| CYP3A4誘導作用を有する抗けいれん薬(フェノバルビタール、フェニトイン、カルバマゼピン等) | アンプレナビルの血中濃度を低下させる可能性がある。 | これら薬剤等はCYP3A4を誘導するため、本剤の代謝が促進される。 |
| セイヨウオトギリソウ(St.John's Wort,セント・ジョーンズ・ワート)含有食品 | アンプレナビルの代謝が促進され血中濃度が低下するおそれがあるので、本剤投与時はセイヨウオトギリソウ含有食品を摂取しないよう注意すること。 | |
| デキサメタゾン | アンプレナビルの血中濃度を低下させる可能性がある。 | |
| ラルテグラビル | 本剤1400mg1日2回とラルテグラビル400mg1日2回を併用した場合、アンプレナビルのCmax、AUC、Cminはそれぞれ27%、36%、43%低下し、ラルテグラビルのCmax、AUC、Cminはそれぞれ29%、37%、38%低下した(空腹時投与)。 アンプレナビルの血中濃度が低下し、本剤の効果が減弱するおそれがあるので、ブーストしない本剤とラルテグラビルの併用は推奨されない。本剤とラルテグラビルを併用する場合は、さらに低用量のリトナビルも併用すること。 |
機序不明 |
| マラビロク | 本剤700mg/リトナビル100mg1日2回とマラビロク300mg1日2回を併用した場合、アンプレナビルのCminは36%減少し、マラビロクのAUCは149%増加した。また、本剤1400mg/リトナビル100mg1日1回とマラビロク300mg1日1回を併用した場合、アンプレナビルのCminは15%減少し、マラビロクのAUCは126%増加した。 本剤/リトナビルとマラビロクを併用する場合には、マラビロクの用量を150mg1日2回に減量すること。 |
本剤及びリトナビルのCYP3A4に対する阻害作用により、マラビロクの代謝が阻害される。 |
| テラプレビル | 本剤/リトナビルとテラプレビルの併用により、定常状態におけるアンプレナビルとテラプレビルの血中濃度が低下する可能性がある。 | 機序不明 |
| パロキセチン塩酸塩水和物 | パロキセチン塩酸塩水和物の作用が減弱する可能性がある。本剤及びリトナビルとパロキセチン塩酸塩水和物の併用により、パロキセチンの血中濃度が約60%低下したとの報告がある。 | 機序不明 |
|
本剤及びリトナビルと経口避妊薬の併用により、リトナビルの血中濃度の上昇及び経口避妊薬の血中濃度の低下がみられ、肝トランスアミナーゼの上昇や黄体・卵胞ホルモンレベルの変動がみられる可能性がある。本剤投与時は別の避妊法を行うことが望ましい。なお、本剤及びリトナビルと高用量のエストロゲンやプロゲストゲンを併用した場合のデータは得られておらず、有効性・安全性は確立していない。 | 機序不明 |
HIV感染症を対象とした海外臨床試験において、700例中246例(35.1%)に中等度又は重度の副作用が認められ、その主なものは下痢53例(7.6%)、悪心37例(5.3%)、嘔吐28例(4.0%)であった。
なお、アバカビル硫酸塩錠を併用した試験においては、主な副作用として薬物過敏症が報告されていた。
なお、副作用の頻度については、日本人における臨床試験成績は得られていないため、HIV感染症を対象とした海外臨床試験成績に基づき分類した。また、上記の海外臨床試験では認められていないが、HIVプロテアーゼ阻害剤を含むレジメンで報告されている副作用については頻度不明とした。
以下のような副作用があらわれた場合には、症状に応じて適切な処置を行うこと。
| 1%~10%未満 | 1%未満 | 頻度不明 | |
|---|---|---|---|
| 皮膚 | 発疹、瘙痒 | 紅斑、斑状丘疹性皮疹 | 血管浮腫 |
| 精神神経系 | 頭痛 | ||
| 心臓障害 | 心筋梗塞 | ||
| 消化器 | 下痢、悪心、嘔吐、腹痛 | 鼓腸、口の錯感覚 | |
| 肝臓 | 肝機能検査値異常(AST(GOT)、ALT(GPT)等の上昇) | ||
| 代謝・栄養障害 | 高脂血症 | 体脂肪の再分布/蓄積(胸部、体幹部の脂肪増加、末梢部、顔面の脂肪減少、野牛肩、血清脂質増加、血糖増加)、リパーゼ上昇 | インスリン抵抗性 |
| 腎及び尿路障害 | 腎結石症 | ||
| 全身症状 | 疲労 |
高齢者における薬物動態は検討されていない。高齢者に対し本剤を投与する場合には、患者の肝、腎、及び心機能の低下、合併症、併用薬等を十分考慮し慎重に投与すること。
低出生体重児、新生児、乳児又は2歳未満の幼児に対する安全性は確立していない(使用経験がない)。
本剤に対する解毒剤は知られていない。また、アンプレナビルは高いタンパク結合率を有するため、腹膜透析や血液透析により除去できる可能性は低い。過量投与時には、患者を十分観察し、必要な対症療法を実施すること。
日本人健康成人男性(n=9)に本剤1400mg、本剤1400mgとリトナビル200mg、あるいは本剤700mgとリトナビル100mgを単回経口投与した時の血漿中アンプレナビル濃度推移を図-1に、アンプレナビルの薬物動態パラメータを表-1に示した。アンプレナビルは投与約3時間後に最高血漿中濃度に達し、消失半減期は約6~7時間であった。

図-1 血漿中アンプレナビル濃度の推移(9例の平均値±標準偏差)
| 投与方法 | Cmax (μg/mL) |
Tmax (h) |
t1/2 (h) |
AUC0-∞ (μg・h/mL) |
|---|---|---|---|---|
| 本剤1400mg | 5.79±2.41 | 3.08±1.35 | 6.47±2.98 | 23.05±7.83 |
| 本剤1400mg+リトナビル200mg | 11.12±2.64 | 3.17±1.12 | 7.19±1.86 | 101.20±27.94 |
| 本剤700mg+リトナビル100mg | 6.69±1.89 | 2.89±1.54 | 6.16±1.16 | 50.65±14.49 |
平均値±標準偏差、n=9
本剤は経口投与後、主に消化管上皮において速やかにアンプレナビルと無機リン酸に加水分解される。
健康成人に本剤1400mgを1日2回、本剤1400mgとリトナビル200mgを1日1回、あるいは本剤700mgとリトナビル100mgを1日2回反復経口投与した時の定常状態におけるアンプレナビルの薬物動態パラメータは下記の通りであった。
| 投与方法 | n | Cmax (μg/mL) |
Tmax (h) |
AUC0-24 (μg・h/mL) |
Cmin (μg/mL) |
|---|---|---|---|---|---|
| 本剤1400mg1日2回 | 12 | 4.91±1.94 | 1.8±0.7 | 36.4±12.6* | 0.25±0.12 |
| 本剤1400mg1日1回 +リトナビル200mg1日1回 |
70 | 7.56±2.01 | 2.3±1.1 | 67.3±18.2 | 1.33±0.57 |
| 本剤700mg1日2回 +リトナビル100mg1日2回 |
24 | 6.31±1.72 | 2.0±1.3 | 83.2±27.4* | 2.33±1.13 |
*AUC0-12を2倍した値
平均値±標準偏差
健康成人に本剤1400mgとリトナビル100mgあるいは200mgを、同一被験者にクロスオーバー法により1日1回、14日間併用投与した時の定常状態におけるアンプレナビルの薬物動態パラメータは以下の通りであった。
本剤1400mgに併用するリトナビルの用量にかかわらず、アンプレナビルの薬物動態は同様であった。
| 投与方法 | n | Cmax (μg/mL) |
Tmax (h) |
AUC0-24 (μg・h/mL) |
Cmin (μg/mL) |
|---|---|---|---|---|---|
| 本剤1400mg+リトナビル100mg | 36 | 7.93 (7.25-8.68) |
1.50 (0.75-5.00) |
66.36 (61.06-72.12) |
0.86 (0.74-1.01) |
| 本剤1400mg+リトナビル200mg | 36 | 8.17 (7.58-8.81) |
2.00 (1.00-4.00) |
73.80 (66.93-81.37) |
1.40 (1.19-1.65) |
幾何平均値(95%信頼区間)、Tmax:中央値(範囲)
健康成人に本剤1400mgを経口投与した時の薬物動態は、食事によって影響されなかった。
健康成人とHIV感染症患者を対象とした各薬物動態試験において、本剤及びリトナビル投与後のアンプレナビルの薬物動態に差は認められなかった。
健康成人に本剤を経口投与した時のアンプレナビルの見かけの分布容積は約600Lであった。リトナビルとの併用投与により、アンプレナビルの見かけの分布容積は約40%低下した。
本剤は経口投与後、主に消化管上皮において速やかにアンプレナビルと無機リン酸に加水分解される。アンプレナビルは、主に肝臓においてCYP3A4により代謝される。
本剤とリトナビルを併用投与した場合、リトナビルによる強力なCYP3A4阻害により、アンプレナビルの代謝がリトナビルにより阻害される結果、血漿中アンプレナビル濃度が上昇する。なお、本剤との併用投与で使用されるリトナビルの用量(100mg1日2回あるいは200mg1日1回投与)は、リトナビルの通常臨床用量(600mg1日2回投与)の6分の1であり、本剤とリトナビルを併用投与した場合の抗ウイルス活性は主にアンプレナビルによるものである。
HIV感染症患者に本剤を経口投与した時のアンプレナビルの消失半減期は約8.5時間であった。
本剤とリトナビルを併用投与した時、アンプレナビルの消失半減期は12時間に延長した。
アンプレナビルの主要な消失経路は肝代謝であり、未変化体(アンプレナビル)の尿中排泄率は1%未満であった。健康成人に14C-アンプレナビルを単回経口投与した時の代謝物及び未変化体の尿中排泄率は約14%、糞中排泄率は約75%であった。
2~18歳のHIV感染症患者におけるアンプレナビルの薬物動態は成人と同様であった。
これらの患者における定常状態時のアンプレナビルの薬物動態パラメータを以下に示す。
| 2-5歳 | 6-11歳 | 12-18歳 | ||||
|---|---|---|---|---|---|---|
| n | FPV 30mg/kg | n | FPV 18mg/kg+RTV 3mg/kg | n | FPV 700mg+RTV 100mg | |
| AUC0-24 (μg・h/mL) |
8 | 31.4 (13.7-72.4) |
9 | 93.4 (67.8-129) |
8 | 58.8 (38.8-89.0) |
| Cmax (μg/mL) |
8 | 5.00 (1.95-12.8) |
9 | 6.07 (4.40-8.38) |
8 | 4.33 (2.82-6.65) |
| Cτ (μg/mL) |
17 | 0.454 (0.342-0.604) |
17 | 2.69 (2.15-3.36) |
24 | 1.61 (1.21-2.15) |
FPV:ホスアンプレナビル、RTV:リトナビル
65歳以上の患者において、本剤投与時の薬物動態の検討は行われていない。
腎機能障害患者における検討は行われていないが、腎排泄はアンプレナビルあるいはリトナビルの主要排泄経路ではなく、これらの排泄に対する腎機能障害の影響は少ないと考えられるため、用量調節を行う必要はない。
軽度の肝機能障害(Child-Pugh分類の合計点数:5~6)を有するHIV感染症患者に本剤700mg1日2回/リトナビル100mg1日1回を併用投与した結果、肝機能の正常なHIV感染症患者に本剤700mg1日2回/リトナビル100mg1日2回を併用投与した場合と比較して、血漿中アンプレナビルのCmax及びAUC0-∞はわずかに高く(それぞれ17%及び22%高い)、Cτは同様であった。
中等度の肝機能障害(Child-Pugh分類の合計点数:7~9)を有するHIV感染症患者に本剤700mg1日1回/リトナビル100mg1日1回を併用投与した結果、肝機能の正常なHIV感染症患者に本剤700mg1日2回/リトナビル100mg1日2回を併用投与した場合と比較して、血漿中アンプレナビルのCavg、Cτ及び非結合アンプレナビルのCτは、それぞれ24%、65%及び42%低かった。
重度の肝機能障害(Child-Pugh分類の合計点数:10~13)を有するHIV感染症患者に本剤300mg1日2回/リトナビル100mg1日1回を併用投与した結果を本剤700mgに標準化し、肝機能の正常なHIV感染症患者に本剤700mg1日2回/リトナビル100mg1日2回を併用投与した場合と比較すると、アンプレナビルのAUC0-τが約80%増加することが示された。
また、肝機能障害患者に本剤を単独投与した時の薬物動態成績は得られていない。しかしながら、肝機能障害患者に対するアンプレナビル600mgの単回経口投与において、中等度の肝硬変患者のAUC0-∞(25.76μg・h/mL)は、健康成人(12.00μg・h/mL)と比較して有意に高値を示した。また、重度の肝硬変患者のAUC0-∞及びCmax(AUC0-∞:38.66μg・h/mL、Cmax:9.43μg/mL)は、健康成人(AUC0-∞:12.00μg・h/mL、Cmax:4.90μg/mL)と比較して有意に高値を示した。
本剤は体内においてアンプレナビルに変換された後、主に肝臓においてCYP3A4により代謝される。また、アンプレナビルはCYP3A4の阻害作用を有する。
本剤又は本剤とリトナビルを併用薬剤と投与した時の薬物動態パラメータの変化を以下に示す。
| 併用薬剤 | 併用薬剤の用量 (mg) |
本剤の用量 (mg) |
n | アンプレナビルの薬物動態 パラメータの変化率(%) |
||
|---|---|---|---|---|---|---|
| Cmax | AUC | Cmin | ||||
| 抗ウイルス化学療法剤(非ヌクレオシド系逆転写酵素阻害剤) | ||||||
| エファビレンツ | 600 QD,2週間 | 1400 QD+リトナビル200 QD,2週間 | 16 | ⇔ | ↓13 | ↓36 |
| エファビレンツ | 600 QD,2週間 | 700 BID+リトナビル100 BID,2週間 | 16 | ⇔ | ⇔ | ↓17 |
| ネビラピン | 200 BID,2週間注1) | 1400 BID,2週間 | 17 | ↓25 | ↓33 | ↓35 |
| ネビラピン | 200 BID,2週間注1) | 700 BID+リトナビル100 BID,2週間 | 17 | ⇔ | ↓11 | ↓19 |
| 抗ウイルス化学療法剤(HIVプロテアーゼ阻害剤) | ||||||
| アタザナビル | 300 QD,10日間 | 700 BID+リトナビル100 BID,10日間 | 22 | ⇔ | ⇔ | ⇔ |
| ロピナビル/リトナビル | 533/133 BID,2週間 | 1400 BID,2週間 | 18 | ↓13注2) | ↓26注2) | ↓42注2) |
| ロピナビル/リトナビル | 400/100 BID,2週間 | 700 BID+リトナビル100 BID,2週間 | 18 | ↓58 | ↓63 | ↓65 |
| 抗ウイルス化学療法剤(HIVインテグラーゼ阻害剤) | ||||||
| ラルテグラビル(空腹時) | 400 BID,2週間 | 1400 BID,2週間 | 14 | ↓27 | ↓36 | ↓43 |
| 抗ウイルス化学療法剤(CCR5阻害剤) | ||||||
| マラビロク | 300 BID,10日間 | 700 BID+リトナビル100 BID,10日間 | 14 | ↓34 | ↓35 | ↓36 |
| マラビロク | 300 QD,10日間 | 1400 QD+リトナビル100 QD,10日間 | 14 | ↓29 | ↓30 | ↓15 |
| 制酸剤 | ||||||
| 水酸化アルミニウム/水酸化マグネシウム | 3600/1800 (30mL),単回 | 1400,単回 | 30 | ↓35 | ↓18 | ↑14 |
| H2受容体拮抗剤 | ||||||
| ラニチジン | 300,単回 | 1400,単回 | 30 | ↓51 | ↓30 | ⇔ |
| HMG-CoA還元酵素阻害剤 | ||||||
| アトルバスタチン | 10 QD,4日間 | 700 BID+リトナビル100 BID,2週間 | 16 | ⇔ | ⇔ | ⇔ |
| アトルバスタチン | 10 QD,4日間 | 1400 BID,2週間 | 16 | ↓18 | ↓27 | ↓12 |
| 抗けいれん薬 | ||||||
| フェニトイン | 300 QD,10日間 | 700 BID+リトナビル100 BID,10日間 | 13 | ⇔ | ↑20 | ↑19 |
| 経口避妊薬 | ||||||
| エチニルエストラジオール/ノルエチステロン* | 0.035/0.5 QD,21日間 |
700 BID+リトナビル注3)100 BID,21日間 | 25 | ⇔ | ⇔ | ⇔ |
↑:上昇,↓:低下,⇔:変化なし(変化率が10%未満)
*:既存データとの比較
注1)試験開始前に少なくとも12週間はネビラピンを投与していた。
注2)本剤700mg BID+リトナビル100mg BID投与時との比較
注3)リトナビルのCmax、AUC、Cminは、それぞれ63%、45%、13%上昇した(他の臨床試験で得られたデータとの比較)。
| 併用薬剤 | 併用薬剤の用量 (mg) |
本剤の用量 (mg) |
n | 併用薬剤の薬物動態 パラメータの変化率(%) |
||
|---|---|---|---|---|---|---|
| Cmax | AUC | Cmin | ||||
| 抗ウイルス化学療法剤(非ヌクレオシド系逆転写酵素阻害剤) | ||||||
| ネビラピン | 200 BID,2週間注1) | 1400 BID,2週間 | 17 | ↑25 | ↑29 | ↑34 |
| ネビラピン | 200 BID,2週間注1) | 700 BID+リトナビル100 BID,2週間 | 17 | ↑13 | ↑14 | ↑22 |
| 抗ウイルス化学療法剤(HIVプロテアーゼ阻害剤) | ||||||
| アタザナビル | 300 QD,10日間 | 700 BID+リトナビル100 BID,10日間 | 21 | ↓24 | ↓22 | ⇔ |
| ロピナビル/リトナビル | 533/133 BID,2週間 | 1400 BID,2週間 | 18 | ⇔注2),注3) | ⇔注2),注3) | ⇔注2),注3) |
| ロピナビル/リトナビル | 400/100 BID,2週間 | 700 BID+リトナビル100 BID,2週間 | 18 | ↑30注2) | ↑37注2) | ↑52注2) |
| 抗ウイルス化学療法剤(HIVインテグラーゼ阻害剤) | ||||||
| ラルテグラビル(空腹時) | 400 BID,2週間 | 1400 BID,2週間 | 14 | ↓29 | ↓37 | ↓38 |
| 抗ウイルス化学療法剤(CCR5阻害剤) | ||||||
| マラビロク | 300 BID,10日間 | 700 BID+リトナビル100 BID,10日間 | 14 | ↑52 | ↑149 | ↑374 |
| マラビロク | 300 QD,10日間 | 1400 QD+リトナビル100 QD,10日間 | 14 | ↑45 | ↑126 | ↑180 |
| HMG-CoA還元酵素阻害剤 | ||||||
| アトルバスタチン | 10 QD,4日間 | 700 BID+リトナビル100 BID,2週間 | 16 | ↑184 | ↑153 | ↑73 |
| アトルバスタチン | 10 QD,4日間 | 1400 BID,2週間 | 16 | ↑304 | ↑130 | ↓10 |
| 抗けいれん薬 | ||||||
| フェニトイン | 300 QD,10日間 | 700 BID+リトナビル100 BID,10日間 | 14 | ↓20 | ↓22 | ↓29 |
| オピオイド受容体作動薬 | ||||||
| methadone(国内未発売) | 200以下 QD,14日間 | 700 BID+リトナビル100 BID,14日間 | 19 | R-methadone(活性体) | ||
| ↓21 | ↓18 | ↓11 | ||||
| 非結合R-methadone 2時間後血中濃度:⇔ 6時間後血中濃度:⇔ |
||||||
| S-methadone(不活性体) | ||||||
| ↓43 | ↓43 | ↓41 | ||||
| 非結合S-methadone 2時間後血中濃度:⇔ 6時間後血中濃度:↓19 |
||||||
| 経口避妊薬 | ||||||
| エチニルエストラジオール(EE)/ノルエチステロン(NE) | 0.035/0.5 QD,21日間 | 700 BID+リトナビル100 BID,21日間 | 25 | EE:↓28 NE:↓38 |
EE:↓37 NE:↓34 |
EE:ND NE:↓26 |
↑:上昇,↓:低下,⇔:変化なし(変化率が10%未満),ND:定量限界以下であったため評価せず
注1)試験開始前に少なくとも12週間はネビラピンを投与していた。
注2)ロピナビルの薬物動態パラメータの変化率
注3)ロピナビル400mg/リトナビル100mg BID投与時との比較
本剤は体内においてアンプレナビルに変換されるため、参考としてアンプレナビルを各種薬剤と併用投与した時の薬物動態パラメータの変化を以下に示す。
| 併用薬剤 | 併用薬剤の用量 (mg) |
アンプレナビルの用量(mg) | n | アンプレナビルの薬物動態 パラメータの変化率(%) |
||
|---|---|---|---|---|---|---|
| Cmax | AUC | Cmin | ||||
| 抗ウイルス化学療法剤(ヌクレオシド系逆転写酵素阻害剤) | ||||||
| ラミブジン | 150,単回 | 600,単回 | 11 | ⇔ | ⇔ | NA |
| ジドブジン | 300,単回 | 600,単回 | 12 | ⇔ | ↑13 | NA |
| 抗ウイルス化学療法剤(非ヌクレオシド系逆転写酵素阻害剤) | ||||||
| デラビルジン | 600 BID,10日間 | 600 BID,10日間 | 9 | ↑40 | ↑130 | ↑125 |
| 抗ウイルス化学療法剤(HIVプロテアーゼ阻害剤) | ||||||
| インジナビル | 800 TID,2週間(空腹時) | 750又は800 TID,2週間(空腹時) | 9 | ↑18 | ↑33 | ↑25 |
| サキナビル | 800 TID,2週間(食後) | 750又は800 TID,2週間(食後) | 7 | ↓37 | ↓32 | ↓14 |
| ネルフィナビル | 750 TID,2週間(食後) | 750又は800 TID,2週間(食後) | 6 | ↓14 | ⇔ | ↑189 |
| 感染症治療剤 | ||||||
| クラリスロマイシン | 500 BID,4日間 | 1200 BID,4日間 | 12 | ↑15 | ↑18 | ↑39 |
| ケトコナゾール | 400,単回 | 1200,単回 | 12 | ↓16 | ↑31 | NA |
| リファンピシン | 300 QD,4日間 | 1200 BID,4日間 | 11 | ↓70 | ↓82 | ↓92 |
| リファブチン | 300 QD,10日間 | 1200 BID,10日間 | 6 | ⇔ | ↓15 | ↓15 |
↑:上昇,↓:低下,⇔:変化なし(変化率が10%未満)
NA:単回投与試験のため算出せず
| 併用薬剤 | 併用薬剤の用量 (mg) |
アンプレナビルの用量(mg) | n | 併用薬剤の薬物動態 パラメータの変化率(%) |
||
|---|---|---|---|---|---|---|
| Cmax | AUC | Cmin | ||||
| 抗ウイルス化学療法剤(ヌクレオシド系逆転写酵素阻害剤) | ||||||
| ラミブジン | 150,単回 | 600,単回 | 11 | ⇔ | ⇔ | NA |
| ジドブジン | 300,単回 | 600,単回 | 12 | ↑40 | ↑31 | NA |
| 抗ウイルス化学療法剤(非ヌクレオシド系逆転写酵素阻害剤) | ||||||
| デラビルジン | 600 BID,10日間 | 600 BID,10日間 | 9 | ↓47 | ↓61 | ↓88 |
| 抗ウイルス化学療法剤(HIVプロテアーゼ阻害剤) | ||||||
| インジナビル* | 800 TID,2週間(空腹時) | 750又は800 TID,2週間(空腹時) | 9 | ↓22 | ↓38 | ↓27 |
| サキナビル* | 800 TID,2週間(食後) | 750又は800 TID,2週間(食後) | 7 | ↑21 | ↓19 | ↓48 |
| ネルフィナビル* | 750 TID,2週間(食後) | 750又は800 TID,2週間(食後) | 6 | ↑12 | ↑15 | ↑14 |
| 感染症治療剤 | ||||||
| クラリスロマイシン | 500 BID,4日間 | 1200 BID,4日間 | 12 | ↓10 | ⇔ | ⇔ |
| ケトコナゾール | 400,単回 | 1200,単回 | 12 | ↑19 | ↑44 | NA |
| リファンピシン | 300 QD,4日間 | 1200 BID,4日間 | 11 | ⇔ | ⇔ | ND |
| リファブチン | 300 QD,10日間 | 1200 BID,10日間 | 6 | ↑119 | ↑193 | ↑271 |
↑:上昇,↓:低下,⇔:変化なし(変化率が10%未満)
*:既存データとの比較
NA:単回投与試験のため算出せず
ND:定量限界以下であったため評価せず
アンプレナビルの血漿蛋白結合率:約90%(in vitro)
抗HIV薬の治療経験がない18歳以上の患者649例を対象とした無作為オープン比較試験(アバカビル300mg1日2回とラミブジン150mg1日2回の併用による、本剤1400mg1日1回/リトナビル200mg1日1回投与群322例又はネルフィナビル1250mg1日2回投与群327例)において、48週間の治療期間中に血漿中のHIV-1 RNA量が検出限界(400copies/mL)未満であった患者の推移を図-2に示した。48週間の治療により、検出限界未満の患者の比率は本剤/リトナビル投与群で69%、ネルフィナビル投与群で68%となり、同等であった。血漿中HIV-1 RNA量が50copies/mL未満の患者の比率もそれぞれ58%、55%であった。48週間の治療後のCD4リンパ球数の増加量(中央値)は、本剤/リトナビル群で203/mm3、ネルフィナビル群で207/mm3であった。
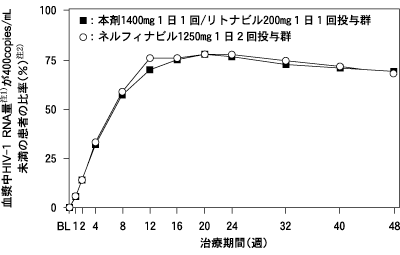
注1)Roche AMPLICOR MONITOR assay(Version 1.5)
注2)中断、データ欠測、リバウンドはHIV-1 RNA量が400copies/mL以上とみなした
図-2 血漿中HIV-1 RNA量が400copies/mL未満の患者の比率
なお、本試験における試験成績の要約を表-9に示した。
| 結果 | 本剤1400mg1日1回/リトナビル200mg1日1回 + アバカビル+ラミブジン (n=322) |
ネルフィナビル1250mg1日2回 + アバカビル+ラミブジン (n=327) |
|---|---|---|
| レスポンダー注1) | 69%(58%) | 68%(55%) |
| ウイルス学的な治療失敗注2) | 6% | 16% |
| 死亡 | 1% | 0% |
| 有害事象による中止 | 9% | 6% |
| その他の理由による中止注3) | 15% | 10% |
(n=Intent-to-treat-analysis)
注1)血漿中HIV-1 RNA量が400copies/mL未満、()内の値は血漿中HIV-1 RNA量が50copies/mL未満
注2)リバウンドを起こした患者、48週を通じてHIV-1 RNA量が減少しなかった患者
注3)同意の撤回、試験途中でフォローアップ不可、プロトコール違反、データ欠測等
ウイルス学的な治療失敗を伴うHIVプロテアーゼ阻害剤の投与経験(2種類以下)がある患者315例を対象とした無作為オープン比較試験において、本剤700mg1日2回/リトナビル100mg1日2回投与群107例、本剤1400mg1日1回/リトナビル200mg1日1回投与群105例、ロピナビル/リトナビル400mg/100mg1日2回投与群103例を比較した。前治療としての逆転写酵素阻害剤の治療期間の中央値(3種類以上の治療経験患者の割合)はそれぞれ257週間(79%)、234週間(70%)、210週間(64%)であり、HIVプロテアーゼ阻害剤の治療期間の中央値(2種類以上の治療経験患者の割合)はそれぞれ149週間(49%)、149週間(57%)、130週間(40%)であった。48週間の治療により、血漿中のHIV-1 RNA量が400copies/mL未満(50copies/mL未満)であった患者の比率は本剤1日2回投与群で58%(46%)、本剤1日1回投与群で50%(37%)、ロピナビル投与群で61%(50%)であった。また、48週間の治療後のCD4リンパ球数の増加量(中央値)はそれぞれ81/mm3、61/mm3、91/mm3あった。
なお、本試験における試験成績の要約を表-10に示した。
| 結果 | 本剤700mg1日2回 /リトナビル 100mg1日2回 (n=107) |
本剤1400mg1日1回 /リトナビル 200mg1日1回 (n=105) |
ロピナビル/リトナビル 400mg/100mg1日2回 (n=103) |
|---|---|---|---|
| レスポンダー注1) | 58%(46%) | 50%(37%) | 61%(50%) |
| ウイルス学的な治療失敗注2) | 29% | 41% | 27% |
| 死亡 | <1% | 0% | 0% |
| 有害事象による中止 | 5% | 2% | 7% |
| その他の理由による中止注3) | 9% | 8% | 5% |
(n=Intent-to-treat-analysis)
注1)血漿中HIV-1 RNA量が400copies/mL未満、()内の値は血漿中HIV-1 RNA量が50copies/mL未満
注2)リバウンドを起こした患者、ウイルス学的効果が不十分のため投与を中止した患者、48週を通じてHIV-1 RNA量が減少しなかった患者
注3)同意の撤回、試験途中でフォローアップ不可、プロトコール違反等
抗HIV薬の治療経験がない17歳以上の患者249例を対象とした無作為オープン比較試験(アバカビル300mg1日2回とラミブジン150mg1日2回の併用による、本剤1400mg1日2回投与群166例又はネルフィナビル1250mg1日2回投与群83例)において、48週間の治療により、血漿中HIV-1 RNA量が検出限界未満(400copies/mL未満)の患者の比率は本剤投与群で66%、ネルフィナビル投与群で52%であった。血漿中HIV-1 RNA量が50copies/mL未満の患者の比率ではそれぞれ57%、42%であった。48週間の治療後のCD4リンパ球数の増加量(中央値)は、本剤群で201/mm3、ネルフィナビル群で216/mm3であった。
なお、本試験における試験成績の要約を表-11に示した。
| 結果 | 本剤1400mg1日2回 + アバカビル+ラミブジン (n=166) |
ネルフィナビル1250mg1日2回 + アバカビル+ラミブジン (n=83) |
|---|---|---|
| レスポンダー注1) | 66%(57%) | 52%(42%) |
| ウイルス学的な治療失敗注2) | 19% | 32% |
| 症状の進行 | 1% | 1% |
| 死亡 | 0% | 1% |
| 有害事象による中止 | 4% | 2% |
| その他の理由による中止注3) | 10% | 10% |
(n=Intent-to-treat-analysis)
注1)血漿中HIV-1 RNA量が400copies/mL未満、()内の値は血漿中HIV-1 RNA量が50copies/mL未満
注2)リバウンドを起こした患者、48週を通じて血漿中HIV-1 RNA量が減少しなかった患者
注3)同意の撤回、試験途中でフォローアップ不可、プロトコール違反、データ欠測等
2~18歳のHIV感染症患者144例を対象とした2つのオープン試験において、これらの患者における本剤の有効性及び安全性が確認された。本剤及びリトナビルの用量については、患者の体重及び年齢に基づき設定した。
上記2試験において、本剤のみを投与された症例はHIVプロテアーゼ阻害剤の投与経験がない患者18例(うち16例は抗HIV薬の治療経験がない患者)、本剤/リトナビルが併用投与された症例はHIVプロテアーゼ阻害剤の投与経験がない患者59例及びHIVプロテアーゼ阻害剤の投与経験がある患者67例であった。24週間の治療により血漿中HIV-1 RNA量が検出限界未満(400copies/mL未満)の患者の比率は、本剤のみを投与されたHIVプロテアーゼ阻害剤の投与経験がない患者で67%(APV29005)、本剤/リトナビルが併用投与されたHIVプロテアーゼ阻害剤の投与経験がない患者でそれぞれ66%(APV20003)、70%(APV29005)、HIVプロテアーゼ阻害剤の投与経験がある患者で2試験ともに57%であった。48週間の治療により血漿中HIV-1 RNA量が検出限界未満(400copies/mL未満)の患者の比率は、HIVプロテアーゼ阻害剤の投与経験がない患者で47%、HIVプロテアーゼ阻害剤の投与経験がある患者で43%であった(APV20003での成績)。
24週間の治療後のCD4リンパ球数の増加量(中央値)は、本剤のみを投与されたHIVプロテアーゼ阻害剤の投与経験がない患者で353/mm3( APV29005)、本剤/リトナビルが併用投与されたHIVプロテアーゼ阻害剤の投与経験がない患者でそれぞれ127/mm3(APV20003)、131/mm3(APV29005)、HIVプロテアーゼ阻害剤の投与経験がある患者でそれぞれ114/mm3( APV20003)、149/mm3(APV29005)であった。48週間の治療後のCD4リンパ球数の増加量(中央値)は、HIVプロテアーゼ阻害剤の投与経験がない患者で163/mm3、HIVプロテアーゼ阻害剤の投与経験がある患者で145/mm3であった(APV20003での成績)。
ホスアンプレナビルは、アンプレナビルのプロドラッグであり、消化管上皮から吸収される過程でアンプレナビルに変換される。
アンプレナビルは、前駆体ポリ蛋白質の解裂に関与するHIVプロテアーゼを阻害することで感染性を持つウイルスの産生を抑制する。
本剤とリトナビルを併用投与した場合、リトナビルによる強力なCYP3A4阻害により、アンプレナビルの代謝がリトナビルにより阻害される結果、血漿中アンプレナビル濃度が上昇する。なお、本剤とリトナビルを併用投与した場合の抗ウイルス活性は主にアンプレナビルによるものである(「薬物動態」の項参照)。
アンプレナビルはMT-4細胞及び末梢血白血球におけるHIV-1 IIIB及びHIV-2 ZYの複製を抑制し、IC50値はそれぞれ80nM及び340nMであった。また、末梢血白血球における臨床分離HIV-1の複製をIC50値12~19nMで抑制した。
アンプレナビルは、ジダノシン、ジドブジン、アバカビル等のヌクレオシド系逆転写酵素阻害剤(NRTI)あるいはサキナビルと併用することにより抗ウイルス活性において相乗作用を示した。また、インジナビル、リトナビルあるいはネルフィナビルと併用することにより相加作用を示した。
HIVをアンプレナビル存在下で培養すると耐性発現の基本となるI50Vの変異及びM46I/L、I47Vの変異がHIVプロテアーゼに生じ、これらの3変異によりアンプレナビルの抗ウイルス活性のIC50値は10倍以上上昇する6)。また、この変異ウイルスをサキナビルの存在下で培養するとI47Vの変異が消失し、サキナビルに対する耐性を獲得すると共にアンプレナビルに対する感受性が回復した7)。一方、インジナビル、ネルフィナビルあるいはリトナビルの存在下ではそれぞれに特有の変異が出現し、2剤に耐性を示すようになる。また、in vitroではI54M、V32I+I47V及びI84Vの変異も同定されている。HIVプロテアーゼ阻害剤(PI)未治療患者において、NRTIであるアバカビル及びラミブジンの治療下でホスアンプレナビルを併用投与すると、17%(5/29例)にアンプレナビル耐性HIVが発現し、55%(16/29例)にNRTI耐性HIVが発現した(APV30001試験)。
同じくPI未治療患者において、NRTI2剤の治療下でネルフィナビルを投与すると31%(17/54例)にネルフィナビル耐性HIVが発現したのに対して、ホスアンプレナビル/低用量リトナビルを併用投与してもアンプレナビル耐性HIVは発現せず(0/32例)、さらに、ホスアンプレナビル/低用量リトナビル併用時のNRTI耐性HIV発現率(13%、4/32例)もネルフィナビル投与時(57%、31/54例)に比較して低かった(APV30002試験)。PI未治療患者におけるアンプレナビル耐性HIVの発現には、I50V、I54L/M、V32I+I47VあるいはまれにI84V変異、さらにそれに続く二次変異としてのM46I/L変異が関与する可能性が示唆されている8)。
アンプレナビルによって発現する変異の組み合わせはアンプレナビルに特有であり、他のPIではみられない。これらの変異HIVはリトナビルに対しては多少の交差耐性を示すものの、サキナビル、インジナビル及びネルフィナビルに対する感受性は変化しない。
PI既治療患者から分離したHIV中の耐性HIVの割合は、アンプレナビルが15%であり最も低かった(ロピナビル22%、サキナビル25%、インジナビル30%、リトナビル35%、ネルフィナビル55%)。また、PIに対して交差耐性を示す変異HIVの74%(322/433株)がアンプレナビルに感受性を示した。アンプレナビルに対する交差耐性に関連する主な変異としてはI84V+L10I/V/Fが考えられている。

レクシヴァ錠700:60錠 瓶
グラクソ・スミスクライン株式会社
〒151-8566 東京都渋谷区千駄ヶ谷4-6-15
ヴィーブヘルスケア・カスタマー・サービス
TEL:0120-066-525(9:00~18:00/土日祝日及び当社休業日を除く)
FAX:0120-128-525(24時間受付)
| おくすりガイド|
おくすりガイド|