ゼリットカプセル15mg,20mgの添付文書

| 商品名: | ゼリットカプセル15 ゼリットカプセル20 |
|---|---|
| 一般名: | サニルブジン |
| 略称 : | d4T |
添付文書の読み方
ここで提供している添付文書情報は、2013年4月17日現在の各医薬品の添付文書を基に作成したものです。書式等については、実際の添付文書と異なるところがあります。添付文書情報は随時更新されます。ご使用の際は、必ず最新の添付文書をご覧下さい。
また、記載されている内容には、専門的な情報が含まれています。文書内の、
この色の文字をクリックすると、別ウィンドウに読み方のアドバイスが表示されます。
この色の文字をクリックすると、別ウィンドウに重大な副作用の解説が表示されます。
この色の文字をクリックすると、別ウィンドウに副作用の症状とその類似語、定義の解説が表示されます。
記載されている情報をご覧になり、疑問などを持たれた場合は、医師・薬剤師にご相談ください。
※このページを開いた時に目次が自動的に表示されなかったときは、ここをクリックしてください。

2013年1月改訂(第19版)
【警告】
【組成・性状】
組成
ゼリットカプセル15は1カプセル中,サニルブジン15mgを含有する。
なお,添加物として結晶セルロース,無水乳糖,乳糖水和物,デンプングリコール酸ナトリウム及びステアリン酸マグネシウム,また,カプセル本体にゼラチン及びラウリル硫酸ナトリウムを含有する。
製剤の性状
| 製剤 | 色 | 内容物 | 形状 | サイズ | 識別コード |
|---|---|---|---|---|---|
| ゼリットカプセル15 | ボディ:黄色 キャップ:褐色 | 白色~黄褐色の粉末 |
|
3号カプセル | BMS 1964 |
| ゼリットカプセル20 | ボディ及びキャップ:淡褐色 | 白色~黄褐色の粉末 |
|
2号カプセル | BMS 1965 |
【効能又は効果】
HIV-1感染症
効能又は効果に関連する使用上の注意
本剤は他に適切な治療法がない場合にのみ使用し,本剤の投与はできる限り短期間とすること。
【用法及び用量】
通常成人には,サニルブジンとして以下の用量を1日2回12時間毎に経口投与する。
- 体重60kg以上:1回40mg
- 体重60kg未満:1回30mg
投与に際しては,必ず他の抗HIV薬と併用すること。
なお,患者の腎機能により減量を考慮する。
用法及び用量に関連する使用上の注意
-
末梢神経障害(四肢のしびれ・刺痛感・疼痛等)があらわれた場合には,投与を中止するなど,適切な処置を行うこと。症状が回復した場合は,以下の用法・用量を参考に投与を開始するなど慎重に投与すること。
- 体重60kg以上の成人では1回20mgを1日2回12時間毎に経口投与する。
- 体重60kg未満の成人では1回15mgを1日2回12時間毎に経口投与する。
- 腎障害のある患者[腎障害のある患者では,本剤の消失半減期が延長し,副作用が強くあらわれるおそれがあるので,以下を参考にして投与量及び投与間隔を調節するなど慎重に投与すること。](「【薬物動態】(5)腎障害者における薬物動態」の項参照)
| クレアチニンクリアランス(mL/分) | サニルブジン投与量・投与間隔 |
|---|---|
| >50 | 通常用量・12時間毎 |
| 26~50 | 通常用量の1/2・12時間毎 |
| ≦25* | 通常用量の1/2・24時間毎 |
※血液透析を受けている患者には血液透析終了後に投与し,透析を行わない日にも同じ時間に投与する。
【使用上の注意】
1.慎重投与
(次の患者には慎重に投与すること)
- 末梢神経障害又はその既往歴のある患者[症状を増悪又は再発させるおそれがある。](〈用法・用量に関連する使用上の注意〉の項参照)
- 肝障害のある患者[症状を増悪させるおそれがある。]
- 腎障害のある患者(〈用法・用量に関連する使用上の注意〉の項参照)
- 膵炎又はその既往歴のある患者[症状を増悪又は再発させるおそれがある。]
2.重要な基本的注意
- 本剤の使用に際しては患者又はそれに代わる適切な者に,次の事項についてよく説明し同意を得た後,使用すること。
- 本剤はHIV感染症の根治療法薬ではないことから,日和見感染を含むHIV感染症の進展に伴う疾病を発症し続ける可能性があるので,本剤投与開始後の身体的状況の変化については,すべて担当医に報告すること。
- 乳酸アシドーシスがあらわれることがあるので,全身倦怠感,悪心・嘔吐,腹痛,急激な体重減少,頻呼吸,呼吸困難,四肢の筋脱力,歩行困難等の症状があらわれた場合には,直ちに担当医に報告すること。
- 末梢神経障害(四肢のしびれ・刺痛感・疼痛等)があらわれることがあり,その発症は投与量に相関していると考えられるので,処方された用量を守ること。また,四肢のしびれ・刺痛感・疼痛等の症状があらわれた場合には,直ちに担当医に報告すること。
- 膵炎があらわれ重篤な転帰をとることがあるので,腹痛,悪心・嘔吐の症状があらわれた場合には,直ちに担当医に報告すること。
- 本剤の長期投与により脂肪組織萎縮症,後天性リポジストロフィー等の発現リスクが上昇すること。
-
乳酸アシドーシスがあらわれることがある。全身倦怠感,悪心・嘔吐,腹痛,急激な体重減少,頻呼吸,呼吸困難,四肢の筋脱力,腱反射消失,歩行困難等が認められた場合には,乳酸アシドーシスを考慮し,投与を中止するなど適切な処置を行うこと。特に,ギラン・バレー症候群に類似した上行性の神経筋脱力は本剤に特徴的な症状であるので注意すること。また,乳酸アシドーシスの症例において,重度の脂肪肝を伴う肝腫大が報告されている。
なお,複数の妊婦において本剤とジダノシンとの併用投与による致死性の乳酸アシドーシスが報告されているので,妊娠期間中の本剤とジダノシンの併用投与は,治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。 - 膵炎があらわれることがあるので,定期的に血清アミラーゼ,血清リパーゼ等の生化学的検査を行うなど,患者の状態を十分に観察し,慎重に投与すること。これらの検査値の上昇がみられた場合には,投与を中止するなど適切な処置を行うこと。また,腹痛,悪心・嘔吐等の膵炎の発症を示唆する臨床症状がみられた場合には直ちに投与を中止し,生化学的検査(血清アミラーゼ,血清リパーゼ等)及び画像診断等による観察を行うこと。
- 抗HIV薬の使用により,体脂肪の再分布/蓄積があらわれることがある。本剤は,他のヌクレオシド系逆転写酵素阻害剤(テノホビル,アバカビル)に比べ脂肪組織萎縮症や後天性リポジストロフィーの発現が多く,その発現と重症度は投与期間に相関しているとの報告がある。また,一旦発症すると本剤から他のヌクレオシド系逆転写酵素阻害剤(テノホビル,アバカビル)に切り替えても改善しない場合があるので,本剤の投与にあたっては,リスクとベネフィットを十分に勘案し,代替の抗HIV薬を慎重に検討すること。また,体脂肪の再分布/蓄積の徴候を判定するための検査を行うなど,脂肪組織萎縮症や後天性リポジストロフィーの徴候に十分注意するとともに,身体状態の変化について定期的に問診すること。
- 本剤を含む抗HIV薬の多剤併用療法を行った患者で,免疫再構築症候群が報告されている。投与開始後,免疫機能が回復し,症候性のみならず無症候性日和見感染(マイコバクテリウムアビウムコンプレックス,サイトメガロウイルス,ニューモシスチス等によるもの)等に対する炎症反応が発現することがある。また,免疫機能の回復に伴い自己免疫疾患(甲状腺機能亢進症,多発性筋炎,ギラン・バレー症候群,ブドウ膜炎等)が発現するとの報告があるので,これらの症状を評価し,必要時には適切な治療を考慮すること。
3.相互作用
併用注意
(併用に注意すること)
| 薬剤名等 | 臨床症状・措置方法 | 機序・危険因子 |
|---|---|---|
| ジドブジン | 細胞内において本剤の活性代謝物であるサニルブジン三リン酸が減少し,本剤の効果が減弱するとの報告があるので,本剤とジドブジンとの併用療法は避けることが望ましい。 | ジドブジンが細胞内における本剤のリン酸化を抑制することが考えられている。 |
4.副作用
〈国内の臨床試験〉
日本国内におけるHIV感染症例を対象とした臨床第I/II相試験において,安全性解析対象80例中副作用が報告されたのは,51例(63.8%)で,主な副作用はLDH上昇(22.5%),AST(GOT)上昇(16.3%),ALT(GPT)上昇(16.3%),貧血(8.8%),悪心・嘔吐(7.5%),食欲不振(7.5%),高脂血症(中性脂肪上昇等)(7.5%),CK(CPK)上昇(7.5%)等であった。重篤な副作用として,本剤との関連性を完全には否定できない尿細管性アシドーシスによる急性腎不全に起因する死亡例が1例報告されている。
国内の拡大臨床試験において,安全性解析対象80例中副作用が報告されたのは,18例(22.5%)で,主な副作用は悪心・嘔吐(3.8%),γ-GTP上昇(3.8%)等であった。
〈使用成績調査〉
使用成績調査の安全性集計対象症例1,853例中の副作用発現率は56.4%であり,主な副作用は,高脂血症(20.5%),肝機能障害(11.0%),末梢神経障害(8.9%),下痢(7.6%),体脂肪の再分布・蓄積(7.3%),尿酸上昇(5.4%),高乳酸血症(4.5%),γ-GTP上昇(4.3%),悪心(4.0%)等であった。
また,1,853例中949例(51.2%)が2年を超えて投与され,長期投与に伴う副作用の発現状況に変化は認められなかった。なお,海外において,本剤の長期投与により脂肪組織萎縮症,後天性リポジストロフィー等の発現リスクが上昇するとの報告がある。
〈海外の臨床試験〉
米国におけるHIV感染症例を対象とした第II相試験(AI455-006試験1)用量0.1,0.5及び2.0※mg/kg/日)において,WHO分類のグレードIII又はIVの副作用が152例中89例(58.6%)に認められた。そのうち減量又は中止を必要とする末梢神経障害は,0.1,0.5及び2.0※mg/kg/日でそれぞれ51例中3例(5.9%),53例中9例(17.0%)及び48例中15例(31.3%)発現した。その他の主な副作用は,うつ病(5.9%),頭痛(4.6%),悪寒・発熱(4.6%),無力症(3.9%),筋肉痛(3.3%),下痢(2.6%),発疹(2.6%)等が認められた。また,グレードIII又はIVの臨床検査値異常はヘモグロビン減少(2.6%),好中球減少(5.3%),血小板減少(3.3%),AST(GOT)上昇(9.2%)及びALT(GPT)上昇(7.9%)等であった。
(※:承認外用量)
また,ジドブジンを6ヵ月以上投与された症例822例を対象に,本剤に切り替えた群とジドブジンを継続して投与した群を比較した第III相二重盲検比較試験(AI455-019試験2))で報告されたサニルブジンを投与された412例中の主な有害事象(本剤との因果関係に関わりなく発現した症状)は,感染(72.1%),頭痛(53.9%),悪寒・発熱(50.2%),無力症(34.7%),腹痛(34.2%),疼痛(20.6%),倦怠感(20.4%),下痢(50.0%),悪心・嘔吐(38.8%),リンパ節症(19.9%),筋肉痛(32.0%),関節痛(22.6%),減量又は中止を必要とする末梢神経障害(13.6%),不眠(29.4%),うつ病(24.0%),不安(21.8%),鼻炎(48.1%),咳(47.3%),咽頭炎(29.9%),発疹(40.0%),アミラーゼ上昇(23.2%)等であった。
FDAのParallel trackガイドラインに従った大規模拡大試験[AI455-900試験3):40mg/日(体重60kg未満は30mg/日)及び80mg/日(体重60kg未満は60mg/日)]において,重篤な有害事象(本剤との因果関係に関わりなく発現した症状)は,11,784例中6,242例(53.0%)に認められた。主な項目は,感染(28.5%:主に日和見感染),死亡(7.2%),新生物(5.1%:主にKaposi肉腫)等であった。死亡は40mg/日群が455例(7.7%),80mg/日群が397例(6.7%)であった。なお,治療の中止を必要とする末梢神経障害は,1,413例(12.0%)であった。WHO分類のグレードIII又はIVの臨床検査値異常は,ヘモグロビン減少(3.5%),好中球減少(12.4%),血小板減少(4.7%),AST(GOT)上昇(6.2%),ALT(GPT)上昇(10.4%),アルカリフォスファターゼ上昇(4.5%)等であった。
「重大な副作用」及び「その他の副作用」の発現頻度は,承認までの国内臨床試験及び使用成績調査2,013例の集計に基づく。海外臨床試験の有害事象については頻度不明とした。
重大な副作用
次のような症状があらわれた場合には,投与を中止するなど適切な処置を行うこと。
(1)乳酸アシドーシス:
乳酸アシドーシス(1.5%)があらわれることがあるので,全身倦怠感,悪心・嘔吐,腹痛,急激な体重減少,頻呼吸,呼吸困難,ギラン・バレー症候群に類似した症状(四肢の筋脱力,腱反射消失,歩行困難,呼吸困難等)等に注意すること。また,乳酸アシドーシスの症例において,重度の脂肪肝を伴う肝腫大が報告されている。
(2)末梢神経障害:
四肢のしびれ・刺痛感・疼痛等の末梢神経障害(8.8%)があらわれることがある。
(3)膵炎:
膵炎(0.4%)があらわれることがあるので,血清アミラーゼ,血清リパーゼ等の生化学的検査を定期的に行うこと。
(4)急性腎不全:
尿細管性アシドーシス等による急性腎不全(0.4%)があらわれることがあるので,定期的に検査を行うなど観察を十分に行うこと。
(5)錯乱,失神,痙攣:
錯乱(頻度不明),失神(0.1%未満),痙攣(0.1%未満)があらわれることがある。
(6)皮膚粘膜眼症候群(Stevens-Johnson症候群):
皮膚粘膜眼症候群(頻度不明)があらわれることがある。
(7)肝機能障害,肝不全:
肝機能障害(10.1%),肝不全(0.2%)があらわれることがあるので,定期的に検査を行うなど観察を十分に行うこと。
その他の副作用
次のような副作用があらわれた場合には,症状に応じて適切な処置を行うこと。
| 種類\頻度 | 5%以上又は*頻度不明 | 0.1~5%未満 | 0.1%未満 |
|---|---|---|---|
| 精神神経系 | ※神経過敏,※思考異常,※自殺企図,※運動失調,※知覚減退,※知覚障害,※偏執反応,※失語症,※歩行異常,※薬物依存 | めまい,異常感覚,不眠,異常な夢,うつ病,傾眠,筋無力症 | 知覚過敏,脳症,不安,言語障害 |
| 消化器 | 下痢(7.1%),※便秘,※鼓腸放屁,※大腸炎,※食道炎,※直腸障害 | 悪心・嘔吐,食欲不振,消化管障害,口内炎,胃炎,消化不良,胃腸出血 | 嚥下障害 |
| 代謝・栄養 | 高脂血症(19.1%),体脂肪の再分布/蓄積(後天性リポジストロフィー,脂肪組織萎縮症,胸部,体幹部の脂肪増加,顔面・末梢部の脂肪減少,クッシング様外見,野牛肩)(6.8%) | 尿酸上昇,LDH上昇,糖尿病,血清アミラーゼ上昇,高血糖,CK(CPK)上昇,低カリウム血症,糖尿,高カリウム血症 | 低ナトリウム血症 |
| 肝臓 | ※胆嚢炎 | γ-GTP上昇,ALT(GPT)上昇,AST(GOT)上昇,ビリルビン上昇,Al-P上昇,肝炎,黄疸,脂肪肝,胆石症 | ウロビリン尿,肝腫 |
| 腎臓 | 血清クレアチニン上昇,蛋白尿,BUN上昇 | 頻尿 | |
| 全身症状 | ※アレルギー反応,※膿瘍 | 感染,倦怠感,発熱,腹痛,新生物(リンパ腫等),頭痛,末梢性浮腫,疼痛,下肢痛 | 悪寒,背部痛,無力症,インフルエンザ様症候群,浮腫,胸痛 |
| 血液・リンパ系 | ※悪性リンパ腫様疾患 | 貧血,血小板減少,白血球減少,好中球減少,好酸球増多,大赤血球症,ヘモグロビン減少,リンパ球増多,単球増多,リンパ節症 | リンパ球減少,好中球増多 |
| 筋骨格 | 筋肉痛,関節痛 | ||
| 呼吸器 | ※肺疾患,※気胸,※鼻炎,※呼吸障害,※副鼻腔炎 | 咳 | 呼吸困難,咽頭炎,肺炎,気管支炎 |
| 皮膚 | ※真菌性皮膚炎,※斑状丘疹性皮疹 | 発疹,そう痒,蕁麻疹,毛嚢炎 | 皮膚乾燥,紅斑性発疹,発汗 |
| 感覚器 | ※耳痛,※視力異常,※網膜炎,※網膜剥離,※盲 | 味覚異常 | |
| その他 | ※末梢性虚血 | 出血,体重減少 | 低血圧,脱水 |
5.高齢者への投与
一般に高齢者では生理機能が低下しているので,減量するなど注意すること。
6.妊婦、産婦、授乳婦等への投与
1.妊婦への投与
- 妊婦又は妊娠している可能性のある婦人には,治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。[複数の妊婦において本剤とジダノシンとの併用投与による致死性の乳酸アシドーシスが報告されている。]
- 動物実験(ラット)では,サニルブジンは胎盤を通じて胎児に移行することが確認されており,胎児組織中濃度は母体血漿中濃度の約60%であった。ヒト出産時胎盤を用いたex vivo試験において,サニルブジンは単純拡散により胎盤を通過することが示唆されている。
2.授乳婦への投与
動物実験(ラット)で,乳汁中に移行することが報告されているので,授乳中の婦人には,授乳を中止させること。
7.小児等への投与
低出生体重児,新生児,乳児,幼児又は小児に対する安全性は確立していない(国内での使用経験がない)。
8.過量投与
成人に長期に過量投与した際,末梢神経障害及び肝機能障害が発現したとの報告がある。サニルブジンは血液透析により除去することができる。
9.その他の注意
- 変異原性試験(染色体異常試験及び小核試験)において変異原性を示したとの報告がある。
- 本剤とヒドロキシウレアが併用されたHIV感染患者で,死亡を含む重篤な膵炎,肝障害及び高度の末梢神経障害が発現したとの報告がある。
【薬物動態】
1.国内(日本人)での成績4)
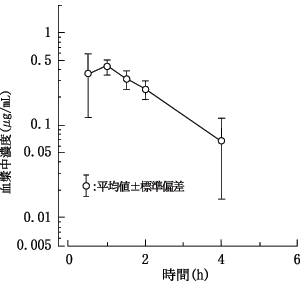
エイズ,エイズ関連症候群患者又は無症候性キャリア(7例)にサニルブジンを経口投与(平均投与量0.59mg/kg)した時の最高血漿中濃度は0.48μg/mLに達し,血漿中半減期は1.35時間であった。尿中回収率(UR)は23.7%であった。日本人におけるサニルブジン投与後の体内動態は外国人と同等であると推察された。
| AUC μg・h/mL |
Cmax μg/mL |
Tmax h |
T1/2 h |
CLT/F mL/min |
UR % |
CLR mL/min |
|---|---|---|---|---|---|---|
| 1.14 (0.26) |
0.48 (0.14) |
0.79 (0.27) |
1.35 (0.27) |
544 (117) |
23.7 (8.4) |
138 (69) |
平均値(標準偏差),n=7
CLT/F:見かけの経口クリアランス
平均投与量:0.59mg/kg
CLR:腎クリアランス
2.(参考)外国人(米国人)による成績
(1)吸収及び生物学的利用率5)~7)
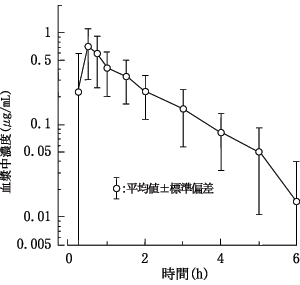
エイズ,エイズ関連症候群患者又は無症候性キャリア(18例)にサニルブジンを経口投与(平均投与量0.57mg/kg)した時の最高血漿中濃度は0.84μg/mLに達し,血漿中半減期は1.39時間であった。尿中回収率(UR)は35.2%であった。
| AUC μg・h/mL |
Cmax μg/mL |
Tmax h |
T1/2 h |
CLT/F mL/min |
UR※ % |
CLR※ mL/min |
|---|---|---|---|---|---|---|
| 1.26 (0.49) |
0.84 (0.34) |
0.70 (0.42) |
1.39 (0.41) |
594 (272) |
35.2 (14.3) |
200 (65) |
平均値(標準偏差),n=18
CLT/F:見かけの経口クリアランス
平均投与量:0.57mg/kg
CLR:腎クリアランス
※:n=14
エイズ,エイズ関連症候群患者又は無症候性キャリア(25例)についてサニルブジンを0.25~4.0mg/kg経口投与し,静注投与時の薬物動態と比較して求めた経口投与時の吸収率(生物学的利用率)は約90%であった。
(2)分布5)~10)
エイズ,エイズ関連症候群患者又は無症候性キャリア(44例)にサニルブジンを0.0625~1.0mg/kg1時間点滴静注(承認外用法用量)した時の見かけの分布容積(Vss)は28.4~81.2Lで,サニルブジンは血管外にも分布することが示された。分布容積は投与量に依存せず,体重にも相関しなかった。
サニルブジンは0.01~11.4μg/mLの濃度で10%以下の血清蛋白結合率を示し,血清蛋白とほとんど結合しない。サニルブジンは赤血球及び血漿に同程度に分布する。
サニルブジンを健常成人(4例)に40mg経口投与した時,投与後約4時間の脳脊髄液内濃度は0.044~0.071μg/mLで,同時点の血漿中濃度の31~45%の値を示し,サニルブジンは脳脊髄液へ移行することが示された。
(3)代謝11)
ヒト肝ミクロゾームを用いたin vitro試験で,サニルブジンからチミン及び極性の高い代謝物が生成し,サニルブジンはピリミジン代謝系等により代謝を受けることが示唆された。なお,ヒトにおけるサニルブジンの代謝は解明されていない。
(4)排泄5)~7)
サニルブジンを0.033~4mg/kg経口投与(110例)後の見かけの全身クリアランスは投与量に依存せず,441~771mL/minであった。腎クリアランスは全身クリアランスの約40%であった。腎クリアランスの平均値は内因性クレアチニンクリアランスの約2倍で,糸球体濾過の他に尿細管分泌もあることが示唆された。経口単回投与後6~24時間までに未変化体として29~44%が尿中に排泄された。
(5)腎障害者における薬物動態12)
低腎機能15例及び正常腎機能5例のHIV非感染者で行った検討では,サニルブジンの見かけの経口クリアランス(CLT/F)はクレアチニンクリアランス(Ccr)の低下に伴って減少し,消失半減期(T1/2)は延長した。
Cmax及びTmaxには腎機能低下による顕著な影響はなかった。これらの知見から,クレアチニンクリアランスの低下した患者ではゼリット(サニルブジン)カプセルの投与量を調節することが望ましい。
| クレアチニンクリアランス | |||
|---|---|---|---|
| >50mL/min (n=10) |
26~50mL/min (n=5) |
9~25mL/min (n=5) |
|
| Ccr(mL/min) | 104±28 | 41±5 | 16±6 |
| CLT/F(mL/min) | 335±57 | 191±39 | 116±25 |
| CLR(mL/min) | 167±65 | 73±18 | 17±3 |
| T1/2(h) | 1.7±0.4 | 3.5±2.5 | 4.6±0.9 |
CLR:腎クリアランス
【臨床成績】
1.国内臨床試験成績
ジドブジン又はジダノシンに効果不十分,不耐容又は不適格なCD4細胞数500cells/mm3以下のHIV感染症例86例を対象とした臨床第I/II相試験における有効性解析対象76例でのCD4細胞数の推移を主とした全般改善度は,改善以上が24週間投与で39.5%(30/76),24週間以上の投与例で13.7%(7/51)であった。
2.海外臨床試験成績
ジドブジンを6ヵ月以上投与された症例822例を対象に,本剤に切り替えた群とジドブジンを継続して投与した群を比較した第III相二重盲検比較試験(AI455-019試験2))では,本剤80mg/日(体重60kg未満は60mg/日:体重換算で1.0mg/kg/日)投与群はジドブジン600mg投与群に比較して,AIDS発症の遅延又は延命(p=0.006),CD4リンパ球数の改善(p<0.0001)においてジドブジンに比較して本剤の有効性が確認された。CD4リンパ球数平均値の推移を示す。
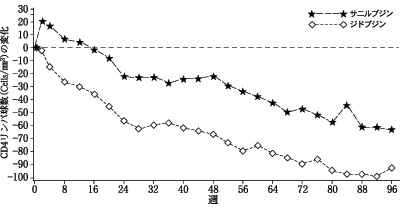
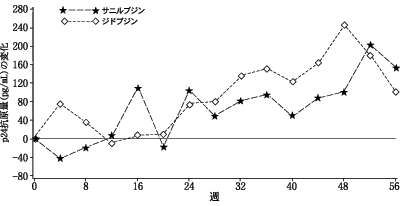
p24抗原量については本剤投与群がジドブジン投与群に比べ,増加は少ないものの有意差はみられなかった(p=0.28)。
【薬効薬理】
1.作用機序13)
サニルブジンはチミジンヌクレオシド類縁体で,in vitroではヒト細胞中のHIVの複製を阻害する。サニルブジンは細胞のキナーゼによってサニルブジン三リン酸となり,抗ウイルス作用を発揮する。サニルブジン三リン酸がHIVの複製を阻害する作用機序としては次の2とおりが知られている。
- 生体中のデオキシチミジン三リン酸と競合してHIV逆転写酵素を阻害する。
- サニルブジンにはDNA鎖伸長のために必要な3'-水酸基が欠落しているので,DNA鎖伸長を終了させてウイルスのDNA合成を阻害する。
2.抗ウイルス作用13)
サニルブジンはHIV-1に感染したT細胞及び単球/マクロファージの細胞培養によるin vitroの試験で抗ウイルス活性を示し(ED50=0.01~4.1μM),HIV-2に対しても抗ウイルス活性を示した(ED50=0.09μM)。
3.薬剤耐性14)
サニルブジンに対する感受性が低下したHIV-1分離株が,細胞培養試験(株特異的)で選別され,また,サニルブジン治療患者からも得られた。サニルブジンの単独投与を6~29ヵ月継続した61名の患者のHIV-1分離株についてその表現型解析を実施した結果,4名の患者で治療後における分離株のEC50値が,治療前ベースラインにおける分離株の平均EC50の4倍以上高値(耐性度7~16倍)を示した。このうち,1名の患者からのHIV-1分離株ではジドブジン耐性関連変異のT215YとK219Eが含まれ,また別の患者の分離株からは,多種核酸系逆転写酵素阻害剤耐性関連変異のQ151Mが含まれていた。残り2名の患者からのHIV-1分離株では,逆転写酵素の遺伝子変異は検出されなかった。サニルブジンに対する感受性変化における遺伝学的な要因は特定されていない。
4.交差耐性15)~17)
サニルブジンの長期間投与によりチミジン類似体耐性変異(TAMs)が発現し,またジドブジンによるTAMs発現後に,サニルブジンを長期間投与した場合にはそのTAMsが継続した。細胞培養試験における感受性の低下は軽微であり,サニルブジン感受性低下(<1/1.5)の前に2ヵ所以上のTAMs(概してM41LとT215Y)を必要とした。これらのTAMsは,サニルブジン及びジドブジンによるウイルス治療において同頻度でみられる。これらの結果は,TAMs,特にM41L及びT215Yが存在する場合にはサニルブジンの治療を避けるべきであることを示唆している。
5.相互作用18),19)
PBMC細胞及びU937株を用いたサニルブジンとジドブジン,リバビリン又はドキソルビシンとのin vitroの併用試験で,サニルブジンの活性代謝物であるサニルブジン三リン酸の生成が有意に抑制されることが報告されている。一方,CEM-SS細胞を用いたin vitroの併用試験で,サニルブジンとジドブジンは相加から拮抗的な抗ウイルス作用が得られたことが報告されている。
【有効成分に関する理化学的知見】
一般名:
サニルブジン(sanilvudine)
略名:
d4T
化学名:
(-)-2',3'-ジデヒドロ-3'-デオキシチミジン
分子式:
C10H12N2O4
分子量:
224.21
構造式:
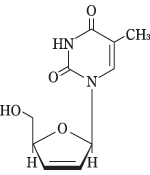
性状:
サニルブジンは白色~微黄白色の結晶又は結晶性の粉末である。N,N-ジメチルアセトアミド,ジメチルスルホキシド又は水にやや溶けやすく,メタノール,エタノール(95)又はアセトニトリルにやや溶けにくく,ジクロロメタンに溶けにくい。
【包装】
ゼリットカプセル15:60カプセル(瓶入)
ゼリットカプセル20:60カプセル(瓶入)
【主要文献及び文献請求先】
主要文献
- M.Rozencweig et al.:社内資料(1993)
- M.Rozencweig et al.:社内資料(1995)
- M.Rozencweig et al.:社内資料(1995)
- 尾碕千晴:社内資料(1996)
- S.Kaul:社内資料(1993)
- S.Kaul:社内資料(1993)
- S.Kaul:社内資料(1993)
- J.S.Janiszewski:社内資料(1991)
- V.Shah et al.:社内資料(1993)
- B.Christofalo et al.:社内資料(1995)
- K.S.Santone:社内資料(1993)
- D.M.Grasela et al.:社内資料(1994)
- M.J.M.Hitchcock:Antiviral Chem.Chemother.,2,125(1991)
- P-F.Lin et al.:Antiviral Ther.,4,21(1999)
- A.Lafeuillade et al.:AIDS Rev.,5,80(2003)
- J.M.Whitcomb et al.:J Infect Dis.,188,992(2003)
- V.Calvez et al.:Antiviral Ther.,7,211(2002)
- P.G.Hoggard et al.:Antimicrob.Agents Chemother.,41,1231(1997)
- C.A.Deminie et al.:Antimicrob.Agents Chemother.,40,1346(1996)
文献請求先
ブリストル・マイヤーズ株式会社 メディカル情報部
(住所)東京都新宿区西新宿6-5-1
(TEL)0120-093-507
【製造販売業者等の氏名又は名称及び住所】
製造販売元
ブリストル・マイヤーズ株式会社
東京都新宿区西新宿6-5-1
| おくすりガイド|
おくすりガイド|

 Page Top
Page Top