
| 商品名: | ザイアジェン錠300mg |
|---|---|
| 一般名: | アバカビル硫酸塩 |
| 略称 : | ABC |
ここで提供している添付文書情報は、2013年4月17日現在の各医薬品の添付文書を基に作成したものです。書式等については、実際の添付文書と異なるところがあります。添付文書情報は随時更新されます。ご使用の際は、必ず最新の添付文書をご覧下さい。
また、記載されている内容には、専門的な情報が含まれています。文書内の、
この色の文字をクリックすると、別ウィンドウに読み方のアドバイスが表示されます。
この色の文字をクリックすると、別ウィンドウに重大な副作用の解説が表示されます。
この色の文字をクリックすると、別ウィンドウに副作用の症状とその類似語、定義の解説が表示されます。
記載されている情報をご覧になり、疑問などを持たれた場合は、医師・薬剤師にご相談ください。
※このページを開いた時に目次が自動的に表示されなかったときは、ここをクリックしてください。

2013年1月改訂(第16版)
(次の患者には投与しないこと)
本剤は、1錠中にアバカビル硫酸塩351mg(アバカビルとして300mg)を含有する。添加物として結晶セルロース、デンプングリコール酸ナトリウム、ステアリン酸マグネシウム、軽質無水ケイ酸、ヒプロメロース、酸化チタン、トリアセチン、黄色三二酸化鉄、ポリソルベート80を含有する。
本剤は黄色のフィルムコート錠である。
| 販売名 | 識別コード | 表 (直径) |
裏 | 側面 (厚さ) |
質量 |
|---|---|---|---|---|---|
| ザイアジェン錠300mg | GX 623 | 長径:18.4mm 短径:7.2mm |
 |
 6.0mm |
814mg |
HIV感染症
通常、成人には他の抗HIV薬と併用して、アバカビルとして1日量600mgを1日1回又は2回に分けて経口投与する。なお、年齢、体重、症状により適宜減量する。
(次の患者には慎重に投与すること)
(併用に注意すること)
| 薬剤名等 | 臨床症状・措置方法 | 機序・危険因子 |
|---|---|---|
| エタノール | 本剤の代謝はエタノールによる影響を受ける。本剤のAUCが約41%増加したが、エタノールの代謝は影響を受けなかったとの報告がある。本剤の安全性の観点から、臨床的に重要な相互作用とは考えられていない。 | アルコールデヒドロゲナーゼの代謝基質として競合すると考えられている。 |
| methadone (国内未発売) |
methadoneのクリアランスが22%増加したことから、併用する際にはmethadoneの増量が必要となる場合があると考えられる。なお、アバカビルの血中動態は臨床的意義のある影響を受けなかった(Cmaxが35%減少し、tmaxが1時間延長したが、AUCは変化しなかった)。 | 機序不明 |
使用成績調査において、安全性判定対象症例643例中、副作用が報告されたのは306例(47.6%)であり、その主な副作用は高脂血症・血中トリグリセリド増加等の体脂肪の再分布/蓄積141例(21.9%)、悪心39例(6.1%)、発疹37例(5.8%)であった(再審査終了時)。
本剤の投与により、次のような症状が認められている。これらの多くは、一般的に本剤の過敏症の一部として発現することがあるので、過敏症が否定できない場合は本剤の投与を直ちに中止し、決して再投与しないこと。また、これらの症状の1つが発現したために本剤の投与を一旦中止し、その後再投与を行う場合は、入院のもとで慎重に行うこと(「警告」、「重要な基本的注意」、「重大な副作用」参照)。
| 10%以上 | 5%~10%未満 | 5%未満 | |
|---|---|---|---|
| 皮膚 | 発疹 | ||
| 消化器 | 悪心 | 嘔吐、下痢食欲不振 | |
| 精神神経系 | 頭痛 | ||
| その他 | 体脂肪の再分布/蓄積 (胸部、体幹部の脂肪増加、末梢部、顔面の脂肪減少、野牛肩、血清脂質増加、血糖増加) |
疲労感、嗜眠発熱、高乳酸塩血症 |
注1)自発報告又は海外のみで認められている副作用については頻度不明とした。
注2)海外での頻度:0.01%未満
本剤の高齢者における薬物動態は研究されていない。本剤の投与に際しては、患者の肝、腎及び心機能の低下、合併症、併用薬等を十分考慮し慎重に投与すること。
生後3ヵ月未満の乳児に対する安全性は確立していない(使用経験が少ない)。なお、小児等に対し本剤を投与した場合、本剤1日1回投与では、1日2回投与と比較して、曝露量が大きくなる可能性がある(「薬物動態」の項参照)。
臨床試験において本剤1回1200mg又は1日1800mgまで患者に投与され、予測できない副作用は報告されていない。なお、過量に投与された時の影響は知られていない。
本剤による副作用(「副作用」の項参照)の発現を注意深く観察し、必要に応じ、一般的な支持療法を行うこと。なお、本剤が血液透析又は腹膜透析で除去されるかどうかは明らかでない。
PTP包装の薬剤はPTPシートから取り出して服用するよう指導すること。(PTPシートの誤飲により、硬い鋭角部が食道粘膜へ刺入し、更には穿孔をおこして縦隔洞炎等の重篤な合併症を併発することが報告されている。)
HIV感染症患者(n=6)に本剤300mgを単回経口投与した場合の血清中濃度推移を図-1に、薬物動態パラメータを表-1に示した。未変化体の血清中濃度は、本剤投与後約1時間で最高濃度に達し、消失半減期は約1.4時間であった。また、アバカビルの投与後8時間までの投与量に対する尿中排泄率は、1.5~4.2%であった。4)
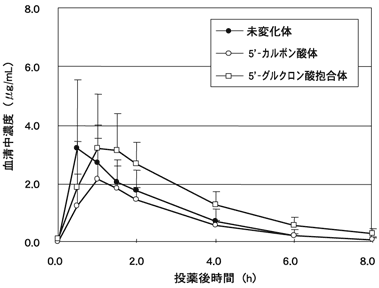
図-1 血清中濃度の推移(6例の平均値及び標準偏差)
| tmax (h) | Cmax (μg/mL) | AUC∞ (μg・h/mL) | t1/2 (h) | |
|---|---|---|---|---|
| アバカビル | 1.0±0.6 | 3.9±1.6 | 8.3±3.5 | 1.4±0.3 |
| 5'-カルボン酸体 | 1.2±0.7 | 2.5±1.2 | 6.3±2.4 | 1.6±0.2 |
| 5'-グルクロン酸抱合体 | 1.2±0.7 | 3.7±1.4 | 12.2±4.3 | 1.9±0.4 |
n=6, 平均値±標準偏差
ラミブジン300mg及びアバカビル600mgを含有する配合剤(エプジコム配合錠)を空腹時単回投与したときのラミブジン、アバカビルの血漿中薬物濃度の推移を図-2及び図-3に、薬物動態パラメータを表-2に示した5)。
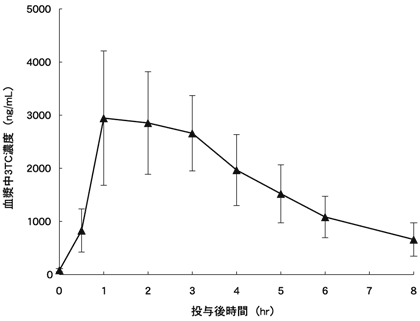
図-2 ラミブジンの血漿中薬物濃度の推移(9例の平均値±標準偏差)
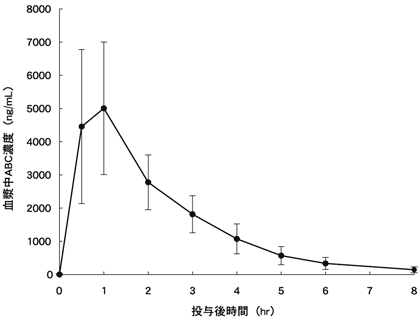
図-3 アバカビルの血漿中薬物濃度の推移(9例の平均値±標準偏差)
| Cmax (μg/mL) | AUClast (h・μg/mL) | AUC0-τ (h・μg/mL) | tmax※ (h) | t1/2 (h) | |
|---|---|---|---|---|---|
| ラミブジン | 3.58 (0.61) |
13.81 (3.56) |
16.30 (5.058) |
2.00 (1.00-3.00) |
2.49 (0.55) |
| アバカビル | 5.68 (2.04) |
12.56 (4.01) |
12.89 (4.22) |
1.00 (0.50-1.03) |
1.50 (0.16) |
N=9、平均値±標準偏差、※中央値(最小値-最大値)
HIV感染症患者(n=12)を対象に本剤100、300、600、900、1200mgを単回経口投与した場合、Cmax及びAUC∞は投与量に依存して上昇した。未変化体の血漿中濃度は投与約1.5時間後に最高濃度に達し、消失半減期は約1.5時間であった6)。
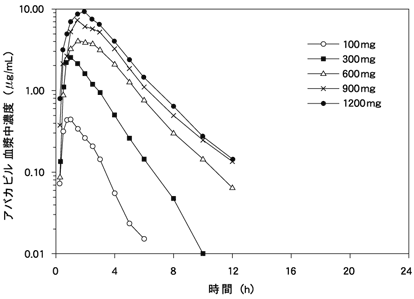
図-4 HIV感染症患者における単回経口投与後の血漿中アバカビル濃度
一方、HIV感染症患者(n=20)を対象に本剤300mgを1日2回投与した場合の定常状態におけるCmaxは約3μg/mL、12時間までのAUCは約6μg・h/mLであった7)。また、生物学的利用率は約83%であった8)。
また、HIV感染症患者(n=27)を対象に本剤600mg 1日1回投与時と本剤300mg1日2回投与時の定常状態における薬物動態パラメータを比較した結果、細胞内カルボビル三リン酸の曝露は、本剤600mg1日1回投与時の方が大きく、AUC0-24、Cmax及びCτがそれぞれ32%、99%及び18%増加した。
HIV感染症患者(n=6)を対象にアバカビルを150mg静脈内投与したときの見かけの分布容積は約0.86L/kgであり、広く組織に分布することが示唆された8),9)。
本薬は10μg/mLまでの添加濃度範囲で、ヒト血漿タンパク結合率は49%と一定であった。また、血液及び血漿中放射能濃度が同じであったことから、本薬は血球に直ちに分布することが示された9)。
HIV感染症患者におけるアバカビルの脳脊髄液(CSF)への移行は良好で、血漿中AUCに対するCSF中AUCの比は30~44%であった9),10)。本剤600mg1日2回投与時の最高濃度の実測値はIC50(0.08μg/mLあるいは0.26μM)の9倍であった9)。
ヒトにおける主要代謝物は、5'-カルボン酸体及び5'-グルクロン酸抱合体であった10)。ヒト肝由来試料を用いたin vitro試験から、本薬は肝可溶性画分により酸化的代謝を受け5'-カルボン酸体を生成したが、肝ミクロソーム画分では本薬の酸化的代謝は起こらなかった。本薬の酸化代謝にはチトクロームP-450ではなく、アルコールデヒドロゲナーゼ/アルデヒドデヒドロゲナーゼ系が関与していた。なお、これらの代謝物には抗ウイルス活性はなかった(社内資料)。
さらに、ヒト肝ミクロゾームを用いたin vitro試験において、臨床使用量での血漿中濃度ではチトクロームP-450分子種CYP2D6, 2C9及び3A4を阻害しないことが示唆された9)。
アバカビルは細胞内で活性代謝物であるカルボビル三リン酸に代謝される。HIV感染症患者(n=20)にアバカビル300mg1日2回投与した時の定常状態における細胞内カルボビル三リン酸の半減期は20.6時間であった(社内資料)。
HIV感染症患者(n=6)を対象に14C標識アバカビル600mgを単回経口投与後、薬物体内動態を検討した。総放射能の約99%が排泄され、主な排泄経路は尿(約83%)であり、糞中には約16%排泄された。尿中に排泄された放射能の約1%は未変化体であり、約30%が5'-カルボン酸体、約36%が5'-グルクロン酸抱合体であった10)。
本薬の主要代謝酵素であるアルコールデヒドロゲナーゼ/アルデヒドデヒドロゲナーゼ系への阻害効果をin vitro試験において検討した結果、本薬自身、これらの酵素を阻害しなかった(社内資料)。
ヒト肝スライスを用いたin vitro試験において、HIVプロテアーゼ阻害薬であるアンプレナビルは本薬の代謝を阻害しなかった(社内資料)。
HIV感染症患者(n=25)を対象に本剤600mgをエタノール0.7g/kgと併用して単回投与した場合、本剤のAUC∞の上昇及びt1/2の延長がみられたが臨床上重要なものではなかった。また、本剤はエタノールの薬物動態に影響を示さなかった11)。
HIV感染症患者(n=15)を対象に本剤600mgとジドブジン(300mg)及びラミブジン(150mg)のどちらか1剤あるいは両剤を併用した場合、いずれの併用においても併用薬による本剤血中濃度への影響はみられなかった。一方、本剤と併用したラミブジンのAUC∞及びCmaxは、ジドブジン併用、非併用に関わらずいずれも低下した。また、本剤と併用したジドブジンは、ラミブジン併用時及び非併用時においてAUC∞の上昇がみられたが、Cmaxは低下した。これらの変化は臨床上重要なものではなかった12)。
HIV感染症患者(n=18)を対象に本剤300mgを食後単回投与した場合、Cmaxは空腹時単回投与と比べ低下したが、AUC∞に変化はみられなかった。
腎疾患患者(GFR:<10mL/min)におけるアバカビルの薬物動態は、腎機能が正常な患者の薬物動態と同様であった。
軽度の肝障害(Child-Pugh 分類の合計点数:5)を有するHIV感染症患者におけるアバカビルの薬物動態を検討した結果、AUC及び消失半減期は肝障害を有さないHIV感染症患者のそれぞれ1.89倍及び1.58倍であった。代謝物の体内消失速度にも変化が認められたが、AUCは肝障害による影響を受けなかった。なお、これら患者に対する推奨投与量は明らかでない。
アバカビルは経口投与後速やかにかつ良好に吸収され、成人と類似した薬物動態が認められる。生後3ヵ月以上で体重30kg未満の小児における推奨用量は8mg/kg1日2回であり、やや高い血漿中濃度が認められるが、成人に300mg1日2回投与した時に得られる血漿中濃度に相当する。
なお、2歳から13歳未満の小児HIV感染症患者を対象とした薬物動態試験において、アバカビル8mg/kg1日2回投与した場合のAUC0-24及びCmaxはそれぞれ9.91μg・h/mL及び2.14mg/Lであり、アバカビル16mg/kg1日1回投与した場合のAUC0-24及びCmaxはそれぞれ13.37μg・h/mL及び4.80mg/Lであった。
生後3ヵ月未満の乳児におけるザイアジェンの推奨用量及び用法は、安全性情報が十分に得られていないため明らかにされていない。現在までに得られている成績から、生後30日未満の新生児にザイアジェン2mg/kg投与した時には、小児に8mg/kg投与した時と類似あるいは高値のAUCがみられることが示されている。
CD4リンパ球数が500/mm3以下のHIV感染症患者16例を対象とした多施設共同オープン試験において、試験開始時のHIV RNA量の平均値は3.41 log10copies/mLであったが、2週後:1.87 log10copies/mL、4週後:1.69 log10copies/mL、8週後:1.38 log10copies/mL、12週後:1.34 log10copies/mL、16週後:1.34 log10copies/mLと、試験開始時から経時的に減少していることが観察され、試験開始時と最終観察時との差は有意であった(p=0.0010 Wilcoxon一標本検定)。
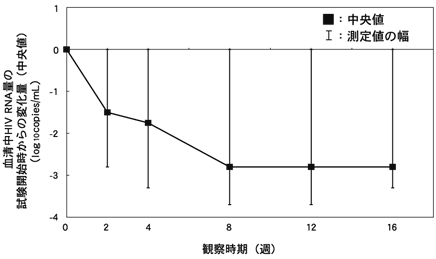
図-5 血清中HIV RNA量の推移(中央値)
また、CD4数の推移をみると、試験開始時の平均値は243.4/mm3、中央値は223.5/mm3であったが、最終観察時(投与後16週)にはCD4数は平均値320.8/mm3、中央値365/mm3に増加した。
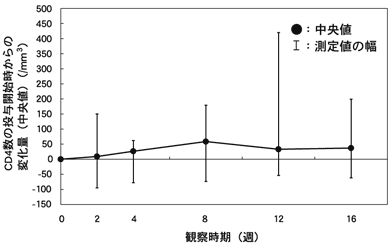
図-6 CD4数の試験開始時からの変化量(中央値)
CD4リンパ球数が100/mm3以上で抗HIV薬による治療経験のない成人HIV感染症患者173例を対象とした二重盲検比較試験において、本剤(300mg1日2回)/ラミブジン(150mg1日2回)/ジドブジン(300mg1日2回)を併用投与した群(本剤併用群)あるいはプラセボ/ラミブジン(150mg1日2回)/ジドブジン(300mg1日2回)を併用投与した群(プラセボ併用群)に、それぞれ87例と86例の患者が無作為に割り付けられた。48週間の治療期間中に、血漿中HIV-1 RNA量が検出限界(400copies/mL)以下であった患者の比率は治療開始8週後より両群間で差がみられ、48週後ではそれぞれ61%と6%となり、プラセボ併用群に比べて本剤併用群の方が高い抗HIV効果を示した。
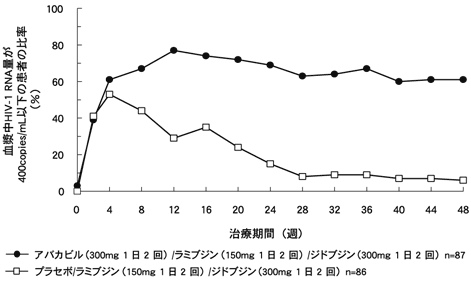
図-7 血漿中HIV-1 RNA量が400copies/mL以下の患者の比率
また、48週後のCD4リンパ球数の増加量(中央値)は、本剤併用群とプラセボ併用群でそれぞれ150/mm3、164/mm3であった。
抗HIV薬による治療経験のある生後3ヵ月~12歳の小児HIV感染症患者205例を対象とした二重盲検比較試験において、アバカビル(8mg/kg1日2回)/ラミブジン(4mg/kg1日2回)/ジドブジン(180mg/m21日2回)を併用投与した群(アバカビル併用群)あるいはプラセボ/ラミブジン(4mg/kg1日2回)/ジドブジン(180mg/m21日2回)を併用投与した群(プラセボ併用群)に、それぞれ102例と103例の患者が無作為に割り付けられた。その結果、48週間の治療期間中に、血漿中HIV-1 RNA量が10000copies/mL以下又は検出限界(400copies/mL)以下であった患者の比率は、治療開始2週後より両群間で差がみられ、48週後ではそれぞれ10000copies/mL以下が36%、26%、検出限界以下が10%、<1%であり、プラセボ併用群に比べてアバカビル併用群の方が高い抗HIV効果を示した。(他剤への変更例を無効とした解析)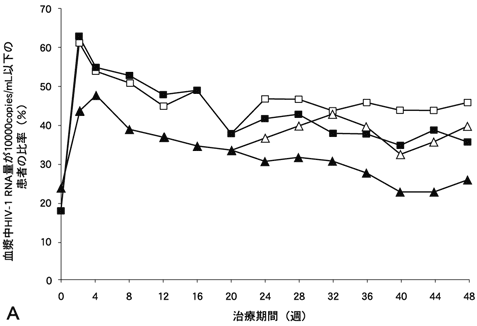

図-8 血漿中HIV-1 RNA量が10000copies/mL以下又は400copies/mL以下の患者の比率
また、48週後のCD4リンパ球数の増加量(中央値)は、プラセボ併用群が-14/mm3と減少したのに対しアバカビル併用群は99/mm3と増加した。なお、48週間を通じてCD4リンパ球数の増加量(中央値)は、アバカビル併用群がプラセボ併用群に比し高値であったが有意差はみられなかった。
治療経験がない成人のHIV感染者770例を対象とした二重盲検比較試験(ラミブジン300mg1日1回とエファビレンツ600mg1日1回の併用による、アバカビル600mg1日1回投与群384例又はアバカビル300mg1日2回投与群386例)を実施した。投与48週後にHIV-1 RNA量が400copies/mL未満であった患者の比率は、アバカビル600mg1日1回投与群、300mg1日2回投与群ともに72%であった。さらに、投与48週後にHIV-1 RNA量が50copies/mL未満であった患者の比率は、アバカビル600mg1日1回投与群が66%、アバカビル300mg1日2回投与群が68%であった(図-9)。
また、投与48週後のCD4リンパ球数の増加量(中央値)は、それぞれ188/mm3、200/mm3であった。
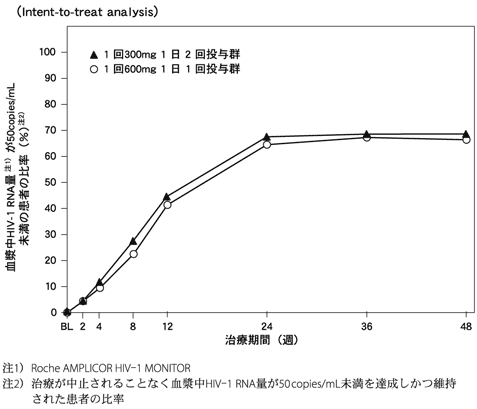
図-9 血漿中HIV-1 RNA量が50copies/mL未満の患者の比率
なお、本試験における試験成績の要約を表-3に示した。
| 結果 | アバカビル600mg1日1回 + ラミブジン+エファビレンツ (n=384) |
アバカビル300mg1日2回 + ラミブジン+エファビレンツ (n=386) |
| レスポンダー注1) | 66%(72%) | 68%(72%) |
| ウイルス学的な治療失敗注2) | 10%(4%) | 8%(4%) |
| 有害事象による中止 | 13% | 11% |
| その他の理由による中止注3) | 11% | 13% |
(n=Intent-to-treat analysis)
注1)血漿中HIV-1 RNA量が50copies/mL未満(400copies/mL未満)となり投与48週後まで維持された患者の比率
注2)血漿中HIV-1 RNA量が50copies/mL未満(400copies/mL未満)となったが投与48週後までにリバウンドを起こした患者、ウイルス学的に治療が失敗した患者、ウイルス学的な効果が不十分と判断された患者
注3)同意の撤回、試験途中でフォローアップ不可、プロトコール違反、症状の進行等
アバカビルは細胞内で細胞性酵素によって活性代謝物のカルボビル三リン酸に変換される。カルボビル三リン酸は天然基質dGTPと競合し、ウイルスDNAに取り込まれることによって、HIV-1逆転写酵素(RT)の活性を阻害する。取り込まれたヌクレオシド誘導体には3'-OH基が存在しないため、DNA鎖の伸長に不可欠な5'-3'ホスホジエステル結合の形成が阻害され、ウイルスのDNA複製が停止する。
アバカビルのHIV-1に対するIC50値はHIV-1 IIIBに対して3.7~5.8μM、臨床分離株に対して0.26±0.18μM(n=8)、HIV-1 BaLに対して0.07~1.0μMであった。また、HIV-2に対するIC50値はHIV-2(Zy)に対して4.1μM、HIV-2 LAV-2に対して7.5μMであった。in vitroでアンプレナビル、ネビラピン及びジドブジンとの併用によって相乗作用が認められ、ジダノシン、ラミブジン、サニルブジン及びザルシタビンとの併用によって相加作用が認められた。また、ヒト末梢血単核球から活性化リンパ球を除いた場合に、より強い抗HIV作用を示したことから、アバカビルは静止細胞でより強く抗ウイルス作用を示すものと考えられる。
アバカビルに対して低感受性のHIV-1分離株がin vitro及びアバカビル投与患者から分離されており、いずれも逆転写酵素にM184V、K65R、L74V及びY115Fの変異が確認された。これらの変異を2種以上含むことにより、アバカビル感受性は1/10に低下した。臨床分離株ではM184V及びL74Vの変異が頻回に観察された。
アバカビルによる耐性逆転写酵素変異を2種以上組み込んだHIV-1株のうち数種は、in vitroでラミブジン、ジダノシン及びザルシタビンに対して交差耐性を示し、一方、ジドブジン及びサニルブジンには感受性を示した。
アバカビルとHIVプロテアーゼ阻害薬とは標的酵素が異なることから、両者間に交差耐性が発生する可能性は低く、非ヌクレオシド系逆転写酵素阻害薬も逆転写酵素の結合部位が異なることから、交差耐性が発生する可能性は低いものと考えられる。
アバカビル硫酸塩(Abacavir Sulfate)
(-)-{(1S,4R)-4-[2-アミノ-6-(シクロプロピルアミノ)プリン-9-イル]シクロペンタ-2-エニル}メタノール1/2硫酸塩
(C14H18N6O)2・H2SO4
670.74

白色~微黄白色の粉末である。トリフルオロ酢酸に溶けやすく、水にやや溶けやすく、メタノール及びエタノール(95)に溶けにくい。0.1mol/L塩酸試液及び希水酸化ナトリウム試液に溶ける。
約219℃(分解)
1.20(pH 7.1~7.3,1-オクタノール/水)
ザイアジェン錠300mg:100錠(10錠×10)PTP
グラクソ・スミスクライン株式会社
〒151-8566 東京都渋谷区千駄ヶ谷4-6-15
ヴィーブヘルスケア・カスタマー・サービス
TEL:0120-066-525(9:00~18:00/土日祝日及び当社休業日を除く)
FAX:0120-128-525(24時間受付)
ヴィーブヘルスケア株式会社
東京都渋谷区千駄ヶ谷4-6-15
http://glaxosmithkline.co.jp/viiv/index.html
グラクソ・スミスクライン株式会社
東京都渋谷区千駄ヶ谷4-6-15
http://www.glaxosmithkline.co.jp
■過敏症を注意するカード
(表面)
(中面)
(裏面)
| おくすりガイド|
おくすりガイド|