
| 商品名: | ハイビッド錠0.375 |
|---|---|
| 一般名: | ザルシタビン |
| 略称 : | ddC |
ここで提供している添付文書情報は、2007年11月1日現在の各医薬品の添付文書を基に作成したものです。書式等については、実際の添付文書と異なるところがあります。添付文書情報は随時更新されます。ご使用の際は、必ず最新の添付文書をご覧下さい。
また、記載されている内容には、専門的な情報が含まれています。文書内の、
この色の文字をクリックすると、別ウィンドウに読み方のアドバイスが表示されます。
この色の文字をクリックすると、別ウィンドウに重大な副作用の解説が表示されます。
この色の文字をクリックすると、別ウィンドウに副作用の症状とその類似語、定義の解説が表示されます。
記載されている情報をご覧になり、疑問などを持たれた場合は、医師・薬剤師にご相談ください。
このページを開いた時に目次が自動的に表示されなかったときは、ここをクリックしてください。
抗ウイルス化学療法剤
Hivid
ザルシタビン(別名:ジデオキシシチジン、ddC)製剤
2005年10月改訂(第7版)
日本標準商品分類番号
87625
| 承認番号 | 08AMY0175 |
| 薬価収載 | 1996年4月 |
| 販売開始 | 1996年4月 |
規制区分:劇薬、指定医薬品、処方せん医薬品 注1)
注1)注意ー医師等の処方せんにより使用すること
貯法:遮光、室温保存、吸湿注意
使用期限:3年(外箱に表示の使用期限内に使用すること)
| 販売名 | ハイビッド錠0.375 | ||
|---|---|---|---|
| 成分(1錠中) | 有効成分・含有量 | ザルシタビン 0.375mg |
|
| 添加物 | 無水乳糖、結晶セルロース、クロスカルメロースナトリウム、褐色酸化鉄、ステアリン酸マグネシウム、ヒドロキシプロピルメチルセルロース、酸化チタン、ポリエチレングリコール、ポリソルベート80、黄色三二酸化鉄、三二酸化鉄、黒酸化鉄 | ||
| 色・剤形 | 淡赤灰色フィルムコート錠 | ||
| 外形 | 平面 | 側面 | |
 |
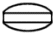 |
||
| 長径 | 約11.5mm | ||
| 短径 | 約5.4mm | ||
| 厚さ | 約3.9mm | ||
| 平均重量 | 約206mg | ||
○治療前のCD4リンパ球数500/mm3以下の症候性及び無症候性HIV感染症
| 薬剤名等 | 臨床症状・措置方法・機序・危険因子 |
|---|---|
| イセチオン酸ペンタミジン (ベナンバックス) |
海外で本剤との併用により劇症 膵炎による死亡例が報告されている。 |
| 薬剤名等 | 臨床症状・措置方法・機序・危険因子 |
|---|---|
| クロラムフェニコール、シスプラチン、ジスルフィラム、エチオナミド、ヒドララジン、イソニアジド、メトロニダゾール、フェニトイン、ビンクリスチン | 作用が相互に増強され、末梢神経障害が発現するおそれがある。 |
| 金製剤 金チオリンゴ酸ナトリウム オーラノフィン 等 |
|
| アムホテリシンB、プロベネシド、シメチジン | 本剤の腎クリアランスを低下させ、 末梢神経障害や他の副作用の発現を増加させるおそれがある。 |
| アミノグリコシド系抗生物質 カナマイシン ゲンタマイシン 等 |
|
| マグネシウム又はアルミニウムを含有する制酸剤 酸化マグネシウム 乾燥水酸化アルミニウムゲル 等 |
本剤の吸収率を低下させるおそれがある。 |
| ジダノシン | 副作用が相互に増強され、 末梢神経障害、膵炎が発現するおそれがある。 |
| ラミブジン含有製剤 | 細胞内におけるザルシタビン及びラミブジンの三リン酸化体が減少し、両剤の効果が減弱する可能性があると報告されているので、本剤とラミブジンとの併用療法は避けることが望ましい。細胞内におけるリン酸化が競合的に阻害されることが考えられている。 |
国内における承認時迄及び使用成績調査81例において、副作用は43例(53.1%)に認められた。主な副作用は、LDH上昇11件(13.6%)、AST(GOT)上昇9件(11.1%)、ALT(GPT)上昇9件(11.1%)、血清アミラーゼ上昇7件(8.6%)、赤血球減少(症)5件(6.2%)、白血球減少(症)5件(6.2%)、好酸球増多(症)5件(6.2%)等であった。(第2回安全性定期報告時)また、米国臨床第II/III相及び拡大適応試験4,660例において、2,202例(47.3%)に、米国臨床第III相試験におけるジドブジンとの併用療法423例において、125例(29.6%)に副作用が認められた。主な副作用は、末梢神経障害、潰瘍性口内炎、嘔気(悪心)、皮疹、好中球減少、白血球減少、貧血、AST(GOT)上昇、ALT(GPT)上昇等であった。
(1%以上注2)又は頻度不明)
次のような副作用があらわれた場合には、投与を中止するなど適切な処置を行うこと。
次のような副作用があらわれた場合には、症状に応じて適切な処置を行うこと。
| 1%以上注2) | 頻度不明 | |
|---|---|---|
| 精神神経系 | 頭痛、抑うつ | ふらつき、緊張亢進、 振戦、攣縮、運動失調、協調異常、言語障害、音声障害、多動、寡動、偏頭痛、神経痛、神経炎、眩暈、集中力低下、性欲減退、健忘、傾眠、不安、不眠、激越、神経過敏、躁状態、多幸症、離人症 |
| 消化器 | 口内炎(アフタ性、潰瘍性)、悪心、嘔吐、腹痛、下痢、便秘 | 食欲不振、嚥下困難、消化管潰瘍、消化管出血、舌潰瘍、食道痛、歯肉疾患、口渇、唾液増加、唾液腺腫大、消化不良、鼓腸、腹部膨満感、おくび、大腸炎、直腸痛、肛門痛、痔疾、血便 |
| 膵臓 | 血清アミラーゼ値の上昇 | 血清リパーゼ値、トリグリセライド値の上昇、血清カルシウム値の減少 |
| 肝臓 | AST(GOT)、ALT(GPT)、Al-Pの上昇 | γ-GTP、LDHの上昇、黄疸、肝炎、肝腫、胆嚢炎、Al-P減少 |
| 循環器 | 心悸亢進、不整脈、心房細動、頻脈、高血圧、失神 | |
| 過敏症 | 発疹、そう痒、蕁麻疹 | 光線過敏症 |
| 腎臓 | 腎嚢胞、腎結石、BUN、クレアチニンの上昇、蛋白尿、排尿困難、尿閉、膀胱痛、頻尿、多尿 | |
| 呼吸器 | 咳、鼻炎、チアノーゼ、咽頭炎、呼吸困難、喀血、胸部うっ血、副鼻腔炎、ラ音、喘鳴 | |
| 血液 | 貧血、白血球減少、好中球減少、血小板減少、好酸球増多 | MCV上昇、リンパ節症、鼻出血、紫斑、血栓、顆粒球増多、ヘモグロビン血症、血小板変化、白血球変化 |
| 内分泌 | 血糖上昇 | 血糖低下、痛風、高尿酸血症、低リン酸塩血症、多飲症、高脂血症、高コレステロール血症 |
| 皮膚 | 皮膚炎、皮膚乾燥、脱毛、紅斑性発疹、ざ瘡、水疱性皮疹、フレグモーネ、口唇疱疹、膿疱性皮疹、カンジダ症、爪の異常、皮膚亀裂、皮膚潰瘍 | |
| 筋骨格 | 関節痛、CK(CPK)上昇 | 筋肉痛、関節炎、筋炎、四肢等の疼痛、骨痛、滑液包炎、筋脱力 |
| 感覚器 | 眼球乾燥、視力異常、結膜炎、結膜変色、眼の異常(炎症、そう痒、疼痛、過敏、充血、出血、涙液増加等)、瞳孔調節障害、耳の障害(耳痛、耳鳴等)、味覚倒錯、味覚消失、嗅覚倒錯 | |
| 電解質異常 | 高ナトリウム血症、低ナトリウム血症、高カリウム血症、低カリウム血症、低マグネシウム血症 | |
| その他 | 発熱、疲労 | 悪寒、体重減少、けん怠、無力症、全身浮腫、顔面痛、胸部痛、四肢冷感、インフルエンザ様症状、発汗、潮紅、悪液質、性器の浮腫・そう痒・疼痛、体脂肪の再分布/蓄積(胸部、体幹部の脂肪増加、末梢部の脂肪減少、野牛肩、クッシング様顔貌)注3) |
注2)米国における臨床試験結果による頻度
注3)臨床症状及び臨床検査値(血中脂質、血糖)に注意し、代謝異常が認められた場合には適切な処置を行うこと。
一般に高齢者では生理機能が低下しているので減量するなど注意すること。
(1)動物実験で催奇形作用が報告されているので、妊婦又は妊娠している可能性のある婦人には、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。
〔ラットで、吸収胚数の増加、胎児奇形(400mg/kg/日以上)、胎児体重減少、胎児奇形(眼開存、小下顎症、口蓋裂、小脳症)、出生児の生存率減少、成長抑制(2,000mg/kg/日)、水頭症、学習・記憶能低下等(1,000mg/kg/日)が、マウスで、胎児体重減少、胎児奇形(ラットの奇形と類似)(400mg/kg/日以上)が報告されている。〕
(2)授乳婦に投与する場合には、授乳を避けさせること。〔動物実験(ラット)で乳汁中へ移行することが報告されている。〕
低出生体重児、新生児、乳児、幼児又は小児に対する安全性は確立していない。〔国内での使用経験はない。〕
ヒトリンパ球を用いた染色体異常試験において1.5μg/mL以上の用量で、マウスを用いた小核試験において骨髄毒性を示す投与用量(4,500mg/kg)で、マウスBALB/c-3T3細胞を用いたトランスフォーメーション試験において125μg/mL以上で変異原性を示したとの報告がある。
エイズ又はエイズ関連症候群(ARC)患者9例にザルシタビンとして1回0.75mgを1日3回(8時間間隔)長期経口投与したとき、ザルシタビンは速やかに吸収され、投与後平均1.1時間で最高血漿中濃度約15.5ng/mLを示し、半減期は約1.8時間(8例)であった。
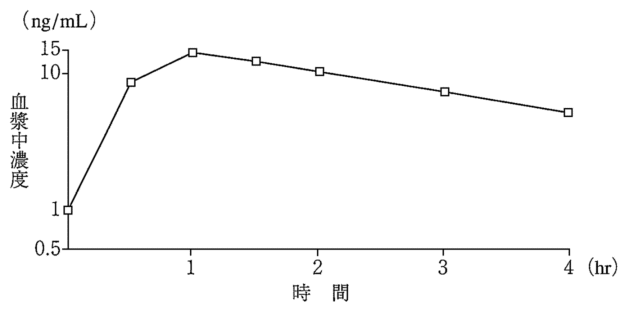
エイズ又はエイズ関連症候群(ARC)患者20例にザルシタビンとして1.5mg(0.375mg×4)を単回経口投与したとき、投与後平均0.8時間で最高血漿中濃度約25.2ng/mLを示し、半減期は約1.9時間であった。
HIV感染患者(n=20)にザルシタビンとして1.5mg(0.375mg×4)を単回投与した際の平均最大血漿中濃度は、絶食時投与の25.2ng/mL(変動係数35%)から、食物摂取後投与の15.5ng/mL(変動係数24%)へと39%減少し、最大血漿中濃度到達時間は絶食時投与の平均0.8時間から食物摂取後投与の平均1.6時間へと約2倍遅延した。AUCは、72ng・hr/mL(変動係数28%)から62ng・hr/mL(変動係数23%)へと14%減少した。これらの変動の臨床的影響は解明されていない。
HIV陽性患者9例にザルシタビンとして(0.06mg/kg又は0.09mg/kg)を4時間ごと、2週間静脈内投与したとき、2週目の投与後2~3.5時間での脳脊髄液濃度は血漿中濃度との比で0.09~0.37(平均0.2)であった。
また、妊娠37~42週での通常分娩又は帝王切開により得られた胎盤での本剤の移行を検討したところ、母側から胎盤へ単純拡散による速やかな移行が認められた。
HIV陽性患者6例に14C-ザルシタビン(1.5mg)を経口投与したとき、投与後120時間までに投与量の76%が尿中に、7.8%が糞中に回収された。なお、そのほとんどは投与後24時間以内に排泄された。また、HIV陽性患者4例に14C-ザルシタビン(1.5mg)を経口投与したとき、投与後48時間までに尿中に排泄された放射能の83%が未変化体ddC、11%が代謝物ddUであった。
国内においてザルシタビンの単独療法並びにジドブジンとの併用療法の2つの臨床試験を実施した。
ジドブジンが無効、不耐容、投与不適格のエイズ又はエイズ関連症候群(ARC)患者24例を対象に、ザルシタビン1回0.75mgを1日3回8時間ごとに24週間投与した。その結果、有効性の評価が可能であった21例中、CD4リンパ球数が投与前値に比較し25/mm3かつ25%以上増加し、それが4週間以上持続した症例は1例(4.8%)、不変の状態を維持した症例は16例(76.2%)であった。また、17例(81.0%)は病勢の進行の指標である日和見感染・悪性新生物の発現がなかった。
CD4リンパ球数が100~500/mm3のHIV感染症患者27例を対象に、ザルシタビン1回0.75mgとジドブジン1回100mgを1日3回8時間ごとに24週間投与した。その結果、有効性の評価が可能であった24例中、CD4リンパ球数が投与前値に比較し25/mm3かつ25%以上増加し、それが4週間以上持続した症例は12例(50.0%)、不変の状態を維持した症例は12例(50.0%)であった。また、21例(87.5%)は病勢の進行の指標である日和見感染・悪性新生物の発現がなかった。
海外におけるザルシタビン単独療法及びジドブジンとの併用療法の臨床試験の結果は、下記の通りであり、ザルシタビンのHIV感染症患者に対する臨床上の有効性が確認された。
ジドブジン前治療歴が1年以上で、投与前CD4リンパ球数<200/mm3、13歳以上のエイズ又はARC患者59例を対象に、ザルシタビン1回0.75mgを1日3回52週間投与した。その結果、死亡あるいはエイズによる日和見感染・悪性新生物の発現を認めた症例は19例(32.2%)であった。死亡例数は10例(16.9%)であり、このうちエイズ患者は9例中2例(22.2%)、ARC患者は50例中8例(16.0%)であった。本剤投与による1年間の推定生存率は81%であった。
また、ジドブジンが無効、不耐容のエイズ又は投与前CD4リンパ球数≦300/mm3、13歳以上のHIV感染症患者237例を対象に、ザルシタビン1回0.75mgを1日3回投与した。その結果、病勢の進行(日和見感染、悪性新生物)例数と死亡例数は、それぞれ115例(48.5%)及び88例(37.1%)であり、1年間あたりの発現率及び死亡率は、それぞれ66.4/100人・年及び35.1/100人・年であった。
18歳以上で、ジドブジン前治療歴のない投与前CD4リンパ球数≦200/mm3のエイズ又はARC患者10例を対象に、ザルシタビン1回0.01mg/kgとジドブジン1回100mgを1日3回投与した。その結果、有効性の評価が可能であった8例で投与後12週においてCD4リンパ球数の増加が7例認められ、そのうち4例は50/mm3以上の増加であった。
また、13歳以上でジドブジン前治療歴が24週以上、投与前CD4リンパ球数≦200/mm3の無症候性HIV感染症患者又は投与前CD4リンパ球数≦300/mm3の症候性HIV感染症患者423例を対象に、ザルシタビン1回0.75mgとジドブジン1回200mgを1日3回投与した。その結果、日和見感染や悪性新生物又は死亡に関する12ヵ月の推定無症状率は73%であり、死亡例数は78例(18.4%)であった。また、併用療法におけるCD4リンパ球数の減少抑制効果、p24抗原量の減少効果はザルシタビン単独療法に比較し、優れた成績を示した。(日本ではジドブジン600mg/日との併用は承認されていない。)
ザルシタビンは天然にあるDNA合成の構成成分の前駆体ヌクレオシド、2'-デオキシシチジンの類似体であり、ヒト免疫不全ウイルス(HIV)感染細胞内で細胞性酵素によりリン酸化され、活性型であるジデオキシシチジン-5'-三リン酸体(ddCTP)になる。ddCTPはウイルスがRNAをDNAへ逆転写するために必須な逆転写酵素を拮抗的に阻害し、また、デオキシシチジン-5'-三リン酸(dCTP)の代わりにウイルス新生DNA中に取り込まれ、ヌクレオチド3'端の3'-水酸基が欠失してDNA鎖伸長を停止することにより、ウイルスの増殖を阻害する。
ザルシタビンはin vitroでヒトTリンパ球及びヒト単球/マクロファージにおけるHIVの複製を通常、0.01~0.5μMで50%阻害(ID50)あるいは95%以上阻害(ID≧95)する。また、ヒトT細胞株ATH8及びMT4培養細胞を用いた系で、ウイルス感染させた細胞を50%防御する濃度(ID50)と非感染細胞(正常細胞)の生細胞数を50%減少させるのに要する濃度(TD50)の比を指標とした選択性指数(TD50/ID50)は175、120と良好な選択性を示した。
ザルシタビン耐性HIV変異株の発現は、逆転写酵素の65番目、69番目、74番目、75番目、184番目及び215番目のアミノ酸変異に関連することが報告されている。
逆転写酵素の69番目のアミノ酸の突然変異は、ザルシタビンに特異的にみられる。また、65番目、74番目、75番目及び184番目の変異はジダノシン(ddI)に対する耐性に関与し、75番目の変異はスタブジン(d4T)に対する耐性と65番目及び184番目の変異はラミブジン(3TC)の耐性に関与している。
HIV逆転写酵素阻害剤とHIVプロテアーゼ阻害剤との交差耐性は薬剤が作用する酵素が異なるため、発現する可能性は低い。
ザルシタビンはin vitroでHIVの正常ヒトT細胞に対する感染及び細胞変性作用を阻害するのに必要な濃度の10~20倍の濃度でも、正常ヒトT細胞のin vitro免疫反応性に対しほとんど影響を与えなかった。
再審査の期間の終了(平成18年4月23日)までの間、本薬が投与された全症例を市販後調査の対象とし、以下の点について重点的に情報の収集・提供に努めること。
また、本薬の使用に当たって患者への十分な説明の上での同意(インフォームド・コンセント)を必ず得るよう投与を行う医師に要請すること。
ハイビッド錠0.375:100錠(バラ)
中外製薬株式会社 医薬情報センター
〒103-8324 東京都中央区日本橋室町2-1-1
電話:0120-189706
Fax:0120-189705
http://www.chugai-pharm.co.jp